単にがんを見つけるだけでなく、どの程度タチが悪いのかを見定めることが大事
肝がんはマーカー、超音波で確定診断。補完的にCTが主流

東京医科大学
内科学第4講座(消化器内科)
主任教授の
森安史典さん
最近の肝がんの検査法の進歩には目を見張るものがある。いち早く病変を見つけるとともに、悪性度をチェックする鑑別診断や、治療と一体化して正確かつ安全な治療をアシストする役割を担うまでになっている。
ほかのがんとは違う発症メカニズムを持つ肝がん
肝がんの大半はC型、B型の肝炎ウイルス感染によるものなので、肝がんのハイリスク患者に的を絞った検査が重要になる。
それは言い換えればハイリスク患者はとくに念入りに検査を受けることでいち早くがんを見つけることが可能ということだ。また最近、肝炎ウイルスとは関係なく、アルコール性肝障害も肝がんの危険因子だが、肥満、糖尿病などのメタボリックシンドロームに合併する非アルコール性脂肪性肝炎(NASH)を原因とする肝がんも増えている。
このような肝がんの危険因子を抱える人は、やはり定期的なチェックが欠かせない。
肝がんの診断は、主に血液検査と画像診断によって行われる。「肝癌診療ガイドライン」によれば、C型肝硬変あるいはB型肝硬変の人(超高危険群)では3~4カ月ごとの超音波検査と腫瘍マーカーの測定、半年から1年ごとのCT(コンピュータ断層撮影)検査またはMRI(核磁気共鳴画像法)検査が推奨されている。また、慢性C型肝炎、慢性B型肝炎、肝硬変の人(高危険群)では、半年ごとの超音波検査と腫瘍マーカーの測定が推奨されている。肝がんの診断にあたっては、まず発症メカニズムの特徴を知ってほしいと語るのは東京医科大学内科学第4講座(消化器内科)主任教授の森安史典さんだ。肝がんの発症メカニズムは、ほかのがんと異なり、「多段階発がん」と「多中心性発がん」という特徴がある。
「多段階発がんとは、最初のうちは前がん病変といえるものでもやがて早期肝細胞になり、高分化肝細胞がん、中分化肝細胞がん、低分化肝細胞がんと悪性度を増していく過程をいいます。悪性度が増すにつれてがんの成長速度は速くなり、浸潤する力も強まって多臓器転移を起こしやすくなります」
多中心性発がんとは、がんがほかの場所に転移するというのではなく、肝臓の中の異なる場所に新しいがんが次々に発生することをいう。“モグラ叩き”や“雨後の竹の子”のように、肝臓全体のあちこちでがんが発生しやすくなっている状態だ。
「そうなると単にがんを見つけるだけでなく、どの程度タチが悪くなっているか、どの段階まで進んでいるかといった診断を早期に行うことが大事になってきます」
腫瘍マーカーは、AFP(アルファフェトプロテイン)、AFP-L3(AFPレクチン分画)、PIVKA-2(異常プロトロンビン)の3種類がある。
このうち、AFPが正常値範囲内でもAFP-L3が陽性なら、がんが疑われる。また、3種類の腫瘍マーカーがいずれも陽性だと悪性度が強いといわれる。ただし、腫瘍マーカーだけでは、たとえがんが発生していても陰性だったり、陽性となっても肝炎や肝硬変などで、がんではない場合もあるため、画像診断との併用が必須だ。
がんの性質、悪性度を識別する新たな造影超音波検査法
腫瘍マーカーと併用して行われる画像診断法のうち最もよく使われるのが、超音波検査。
X線を使わないので放射線の被曝がなく、侵襲がないため安全で手軽な検査という利点がある。ただし、従来の超音波検査では、ある程度の大きさがないと悪性かどうかの判断ができない、などの難点があった。そうした問題を解決し、超音波検査を一挙に進歩させたのがマイクロバブル(微小気泡)を造影剤として使った造影超音波検査である。07年、新たにソナゾイド(一般名ペルフルブタン)というマイクロバブル造影剤が登場してさらに有効性が増した。
「超音波ドプラー検査は、体内を流れる赤血球の速度の違いをキャッチして映像にして描き出します。その映像をさらに明瞭に得られる方法として開発されたのがマイクロバブルを使った造影超音波検査です」
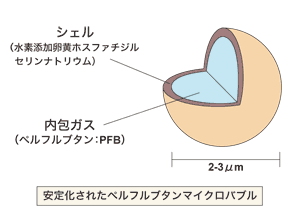
ソナゾイドは直径2~3ミクロン(1ミクロンは1/1千ミリメートル)、赤血球の4分の1の大きさの泡でできているので毛細血管でも楽に通ることができる。泡の膜はリン脂質で作られ、中のガスはフッ化炭素でできており、安全性も高い。静脈から注射すると血流に乗って全身を巡るが、1回に注射する量はわずか0.5㏄。膜は細胞膜と同じ成分なので体内で代謝され、中のガスは呼気を通して対外に排泄される。“体にやさしい”造影剤、といえる。
超音波は気体に反射するため、ソナゾイドを注入した血管は通常の血管に比べ、キラキラ光って見える。がんは、成長していく過程で血流を次第に変化させていく。
肝がんの場合、動脈は増えて門脈(脾臓・消化器からの血液を集めて肝臓に運ぶ静脈)は減っていくので、ソナゾイドを注入すると動脈と門脈で光り方が違うため、がんの存在をキャッチできる。
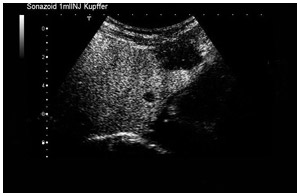
「このような血管イメージをとらえられるのは、注射して最初の1~3分。それから10分後ぐらいからは、今度はクッパーイメージ(肝実質造影)が得られます。肝臓にはクッパー細胞という免疫細胞があり、粒子のある異物を処理する機能をもっています。肝臓に流れてきたマイクロバブルを貪食するので、映像化するとクッパーイメージがとらえられます。ところが、がんの組織は正常組織ではないため、クッパー細胞が存在せず、超音波をあてるとその部分だけが抜けて、黒く映ります」
キラキラ光った肝臓の中に逆のコントラストで黒く抜けて見える部分があれば、そこにがんがあると診断できる。このように、血管イメージとクッパーイメージの両方をとらえることにより、がんの性質を見きわめ、悪性度の鑑別も的確にできるようになったという。ソナゾイドは、もともとノルウェーで開発された。日本は森安さんが中心となって製薬会社と実用化に取り組み、世界に先がけて承認された。
同じカテゴリーの最新記事
- がんゲノム医療をじょうずに受けるために 知っておきたいがん遺伝子パネル検査のこと
- AI支援のコルポスコピ―検査が登場! 子宮頸がん2次検診の精度向上を目指す
- 「尾道方式」でアプローチ! 病診連携と超音波内視鏡を駆使して膵がん早期発見をめざす横浜
- 重要な認定遺伝カウンセラーの役割 がんゲノム医療がますます重要に
- 大腸のAI内視鏡画像診断が進化中! 大腸がん診断がより確実に
- 「遺伝子パネル検査」をいつ行うかも重要 NTRK融合遺伝子陽性の固形がんに2剤目ヴァイトラックビ
- 血液検査で「前がん状態」のチェックが可能に⁉ ――KK-LC-1ワクチン開発も視野に
- 遺伝子変異を調べて個別化の最先端を行く肺がん治療 非小細胞肺がんのMET遺伝子変異に新薬登場
- 自己採取HPV検査とHPVワクチンの持続感染予防効果を検討 〝子宮頸がん撲滅〟を目指す2つの臨床研究~福井大学
- 受診率アップのためには若い世代への意識付けが肝要 大学生に対する子宮頸がん検診啓発活動を実施~福井県



