身体への負担が少ないから術後の回復も早い 9センチのがんも開腹せずに一括切除するITナイフの最新成果

国立がん研究センター中央病院
消化器内視鏡部の
後藤田卓志さん
内視鏡先端からITナイフという電気メスを使って、粘膜に留まるがんであれば、3センチを越える大きなものでも完全に切り取る治療方法が、今、大きな注目を浴びている。画期的ともいえるこの方法は、内視鏡的粘膜下層剥離術(ESD:Endoscopic Submucosal Dissection)と呼ばれ、外科手術で開腹する方法と比べて、患者にやさしい新時代の治療法として次第に普及しつつある。この治療法に早くから着目し、研究・開発を重ねて実用化への可能性を開いた1人、国立がん研究センター中央病院消化器内視鏡部の後藤田卓志さんに、その方法のメリットと実際を語ってもらった。
病変部を大きく剥ぎ取る、ITナイフというすぐれた電気メスの登場
お腹を切らずに内視鏡でがんを電気的に剥ぎ取る手技は、1970年代初頭にドイツ人の医師が大腸のポリープ手術を行ったのが最初です。その後、日本でも研究が進められ、実用化に向けてさまざまに展開されたものの、現実には手詰まりとなっていました。
やがて病変の患部を引っ張る、あるいはつまんでワイヤーで切り取る治療法として、内視鏡的粘膜切除術(以下EMR:Endoscopic Mucosal Resection)という手技が開発されました。
ただし、切除部分の大きさが1センチ、大きくても2センチ以下とされていました。手技がうまくいっても、全体で1.5センチ~2センチぐらいしか取れなかったからです。これは、がん細胞そのものは1センチぐらいしか取れないことを意味しています。
その後、大きな病変はいくつかに分けて切除する方法が考案され、広く浸透してきたのです。これがEMRによる『病変の分割切除法』です。しかし、その方法は、切除方法としてはやや問題があります。大きな病変を分割することで取り残しやがん細胞に傷がつき、散らばってしまう恐れがあるからです。
がんは「細胞1個で生きていける」という定義があります。わずか0.01ミリ程度のがん細胞は、たった1個残っただけで増殖し、局所の再発が起こってきます。実際、再発が10~20パーセントほど見られています。ただ、それ以外に方法がないために、全国でこれまで適用されてきました。

ITナイフ

フックナイフ

フレックスナイフ
病変9センチの周囲を最大13センチ切除。転移なくいずれも根治
そこで、この欠点を解消しようとして、病変部をごっそり剥ぎ取るITナイフというすぐれた電気メスが考案されました。この最新器具を使った手技が、内視鏡的粘膜下層剥離術 (以下ESD:Endoscopic Submucosal Dissection)による『一括切除』です。この方法を使えば、極論して言えば、胃袋の内側をすべて剥ぎ取ることも可能です。
内視鏡手技は、外科手術に携わる医師同様に、繊細でかつ、大胆な手先の器用さが要求されます。胃壁の厚みはわずか7ミリしかありません。そのうちの表層3ミリほどを、モニターを見ながら剥ぎ落とします。微妙でデリケートで、ときに大胆さも必要とされる難しい手技です。
手技に要する時間は2センチ以下の病変であれば20分ほどで終了しますが、大きな病変や困難例では2時間以上にも及ぶ治療になることもあります。これまでの最大切除は13センチの長さのもので、4例あります。がんの病変そのものは9センチ程度でした。このときの手技時間は、平均3時間です。4例が4例とも粘膜の表面だけで留まっていたもので、いずれの患者さんも根治できています。
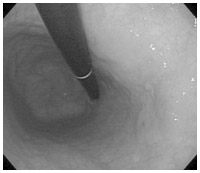
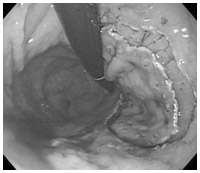
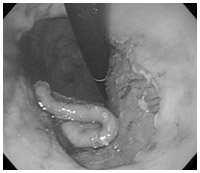
リンパ節転移のない早期がんが内視鏡治療の適用範囲
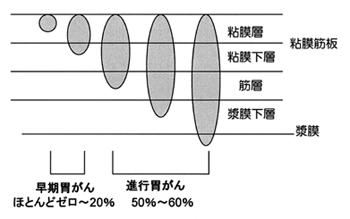
胃壁は、内側から粘膜、粘膜下層、筋層、漿膜下層、漿膜という5層から構成されています。がんは必ず胃の粘膜にできますが、このうち、病変がこの粘膜か、あるいは粘膜下層に留まっているものを早期がんといいます。この場合、リンパ節転移の有無は問いません。これに対して筋層より漿膜まで達しているのが進行がんです。
リンパ節転移は、がんが粘膜下層まで達した場合は、20パーセント程度、さらに進行がんでは50~60パーセントあります。しかし、がんが粘膜内に留まっていれば、これまでの経験と実績により、転移がほとんどないことが分っていましたが、1980年ぐらいまでは、内視鏡による治療が発達していなかったため、このようながんでも、外科手術で胃をそっくり取っていたのです。胃がんに対して根治を目的とした外科手術とは、胃切除とリンパ節郭清です。
しかし、転移がなければリンパ節郭清は必要ありません。ただし“ほとんどゼロ”では困るわけで、確実にゼロパーセントでなければなりません。
そこで、詳細な検討によってある条件を満たした粘膜のがんであればリンパ節転移がないことが解析されました。内視鏡治療の適用が、すなわちこの範囲なのです。
ただし、がんが粘膜に留まっているか、それ以上に進行しているかは、術前には100パーセントは分りません。正確に診断する術がないのです。
同じカテゴリーの最新記事
- 有効な分子標的治療を逸しないために! 切除不能進行・再発胃がんに「バイオマーカー検査の手引き」登場
- 新薬や免疫チェックポイント阻害薬も1次治療から 胃がんと診断されたらまずMSI検査を!
- ビタミンDの驚くべき効果がわかってきた 消化管がん手術後の再発・死亡リスクを大幅に減少
- 薬物療法が奏効して根治切除できれば長期生存が望める ステージⅣ胃がんに対するコンバージョン手術
- 胃がん新ガイドライン「条件付き承認」で増える治療選択 1次治療でオプジーボ承認
- 術後合併症を半減させたロボット支援下手術の実力 胃がん保険適用から3年 国産ロボット「hinotori」も登場
- 適切なタイミングで薬剤を切り替えていくことが大切 切除不能進行・再発胃がんの最新薬物療法
- 術前のスコア評価により術後合併症や全生存率の予測も可能に 進行胃がんに対するグラスゴー予後スコアが予後予測に有用
- ガイドライン作成で内科的治療がようやく整理される コンセンサスがなかった食道胃接合部の食道腺がん
- 新規の併用療法による治療効果改善に期待 ステージⅢ胃がんにおける術後補助化学療法の現状



