渡辺亨チームが医療サポートする:多発性骨髄腫編
渡辺亨チームが医療サポートする:多発性骨髄腫編
金成元さんのお話
*1 多発性骨髄腫の病期
多発性骨髄腫と診断されたら、病気の拡がりや程度(病期)を決めるための詳しい検査が必要です。病期は、治療法の選択や予後の推定に重要であり、現在はDurie & Salmonの分類法と呼ばれるものが最も広く用いられています。これによると、1期、2期、3期の3段階が設けられ、1期は全身の骨髄腫細胞数が対表面積1平方メートル当たり6000億個未満、2期は同じく6000億~1.2兆個、3期は同じく1.2兆以上に相当すると考えられています。そのほか、次のような基準が設けられています。
| ステージ1 | 貧血ではない(ヘモグロビン>10g/dl) 高カルシウム血症ではない(血清カルシウム≦12mg/dl) レントゲン写真上、骨に異常がないか、あっても孤立性の形質細胞腫のみ Mタンパクの量が少ない(IgG<5g/dl、IgA<3g/dl、または尿中軽鎖Mタンパク成分<4g/24時間) |
|---|---|
| ステージ2 | 1期ならびに3期の条件を満たさない場合 |
| ステージ3 | 以下の項目のうちひとつ以上を満たす場合 貧血が強い(ヘモグロビン<8.5g/dl) 高カルシウム血症がある(血清カルシウム>12mg/dl) 進行した骨融解病変を認める(広範囲にわたるか骨折を伴う) Mタンパク量が多い(IgG>7g/dl、IgA>5g/dl、または尿中免疫グロブリン軽鎖Mタンパク成分 (ベンス・ジョーンズ タンパク)>12g/24時間) |
最近ではDurie & Salmon分類に替わる、簡便で利用しやすい分類が模索され、2003年には、ISS(International scoring system)が提唱されました。この方法では、下表のように分類されています。
| ステージ1 | 血清β2ミクログロブリン<3.5mg/lかつ血清アルブミン>3.5g/dl |
|---|---|
| ステージ2 | 血清β2ミクログロブリン>3.5mg/lかつ血清アルブミン<3.5g/dl、 または血清β2ミクログロブリン3.5g/dl~5.5 |
| ステージ3 | 血清β2ミクログロブリン<5.5mg/l |
*2 骨病変への治療
多発性骨髄腫で重度の骨の痛みがある場合は、その骨に対して適切な鎮痛薬と放射線治療を併用することで、痛みを軽減できます。放射線治療には骨の腫瘤を抑えて骨折を予防する効果もあります。パミドロン酸(ビスフォスフォネート系の薬)やさらに強力なゾレドロン酸を1カ月に1回静脈投与すると、骨折、痛み、高カルシウム血症といった骨合併症の発生を抑えることができる上、がんそのものを抑える作用もあるのではないかといわれています。
そこで大多数の患者さんには、副作用がない限り、これらの薬が治療の一部として長期にわたり投与されます。 このほか、骨のケアとして、長期間寝ていると骨量の減少が促進され、骨がもろくなって骨折しやすくなるため、骨を守るために入院中も体を積極的に動かすことも重要です。
ただし、動かし方によっては骨折が悪化することもあるので、医師や理学療法士の指示に従ってください。
*3 多発性骨髄腫の治療の選択
多発性骨髄腫は治療法が近年進歩しているとはいえ、現在のところ根治する方法は見つかっていません。治療の目的は症状の軽減や合併症の予防と緩和、異常な形質細胞の破壊、病気の進行を遅らせることなどです。
多発性骨髄腫が1期などの早期で見つかり、症状が軽微な場合や診断が明確でない場合には、普通、治療を行わずに経過を観察します。根治できる治療が見つかっていないので、臓器がんなどのように早期発見・早期治療は意味があるかどうかわかっていないのです。
しかし、2期や3期の場合は治療をすれば60パーセント以上の割合で病気の進行を遅らせることができることがわかっており、この病期で診断が確定したらなるべく早く治療を開始する必要があります。
治療には、まず化学療法が選択されますが、治療の分岐点になるのはだいたい65歳という年齢です。これより上の方には、昔ながらのMP療法などの化学療法が取り入れられ、これより下の方には、VAD療法という化学療法をしたあと、骨髄腫細胞が作り出すMタンパクが血液や尿の中から消えたことが検査で証明される完全奏効(complete Response ; CR)、あるいはMタンパクが半分以上減る等の部分奏効(partial response ; PR)を目指します。あまり減らない不変(no change ; NC)という状態でVAD療法が終了することもありますが、VAD療法の効果がどうであれ、次に自家移植を併用した大量化学療法による治療に進むのが標準的です。
*4 寛解(あるいは奏効)
血液のがんでは、治療を行ってがん細胞が減る効果が現れることを寛解あるいは奏効と呼びます。
しかし、同じ血液のがんでも、種類によって治療効果判定の基準は大きく異なっています。多発性骨髄腫の治療効果判定はMタンパクの減少を目安にするのが普通です。Mタンパクの減少率が高いと生存率がよくなるという考え方もありますが、必ずしも確定的ではありません。
これ以外に、主に欧米で用いられている「免疫固定法」という検査法を用いて、血清および尿中のMタンパクが消失し、かつ骨髄腫細胞の消失を確認できたTrue Complete Response(真の完全奏効)という基準も設けられています。
| Complete Response(CR)完全奏効 | 75%以上の血清Mタンパクの減少または90%以上の尿中Mタンパクの減少 |
|---|---|
| Partial Response(PR)部分奏効 | 50%以上75%未満のMタンパクの減少 |
| Object Response(OR)具現奏効 | 25%以上50%未満のMタンパクの減少 |
| No Response(NR)不変 | 25%未満のMタンパクの減少 |
| Progressive Disease(PD) | 25%以上のMタンパクの増大 |
*5 自家移植
「血液の工場」である骨髄や末梢血の中に含まれる「血液の種」である造血幹細胞を体外に取り出し冷凍保存しておき、大量の抗がん剤や放射線の全身照射でがん化した骨髄細胞をたたいた後、保存しておいた造血幹細胞を静脈点滴で戻して血液をつくりださせようとする治療が自家移植です。
自家移植自体には治療効果はなく、あくまで大量療法のサポート役を担っています。従来一般的に行われていたMP療法と呼ばれる化学療法では最大で平均生存期間は30カ月でしたが、大量療法+自家移植が取り入れられたことによって、初発の多発性骨髄腫は「完全寛解」が20~40パーセント程度得られるようになり、平均生存年数も4~5年に延びました。
自家移植には、末梢血幹細胞移植と骨髄移植の2つがありますが、骨髄移植よりも末梢血幹細胞のほうが移植後の造血の回復が早いことがわかっており、最近では末梢血幹細胞を用いることが標準になっています。
しかし、自家移植の問題は、移植が成功しても90パーセント以上が再発する点という点です。そこで、計画的に2回続けて大量療法+自家移植を行う「タンデム(馬を縦につなぐという意味)移植」というものが考案されました。フランスで、タンデム移植と1回移植を比較試験した結果、7年生存する骨髄腫の方はそれぞれ42パーセントと21パーセントで、タンデム移植が優れていることがわかっています。
それでも、自家移植は再発しやすいため、再発が少ない(他人からの提供を受ける)同種造血幹細胞移植と、どちらが成績がよいかという比較検討も行われています。その結果、同種移植は、Graft-versus-myeloma(GVM)効果と呼ばれる免疫作用が加わるため、治療効果は優れている場合が多いのですが、移植に伴う合併症による死亡率が高いため、自家移植と同等の成績でした。臨床試験で採用された同種移植の方法自体に問題がありますが、現時点では、65歳以下で全身状態のよい多発性骨髄腫患者さんの治療法の第1選択は、大量療法+自家移植となっています。
*6 VAD療法と自家移植の流れ
VAD療法は、多発性骨髄腫の初期治療で、抗がん剤であるオンコビン(一般名ビンクリスチン)、アドリアシン(一般名塩酸ドキソルビシン)と、副腎皮質ホルモン(ステロイド)剤であるデカドロン(一般名デキサメタゾン)という薬剤を組み合わせて投与する治療法です。
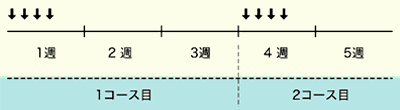
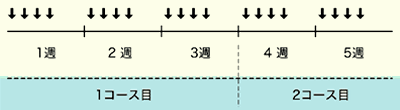
3週間で行う1コースの中で、オンコビンは1日0.4ミリグラムを第1日目~第4日目、アドリアシンは体表面積1平方メートル当たり9あるいは10ミリグラムを第1日目~第4日目、デカドロンは1日20~40ミリグラムを第1日目~第4日目・第8日目~第11日目・第15日目~第18日目にそれぞれ投与します。これを4コース、計12週間で終了することが原則です。
国立がん研究センター中央病院では、VAD療法1コース目の副作用が軽く、患者さんの希望があれば、2コース目以降は最短で4泊5日の入院期間で済み、次のコースでまた入院していただくということを繰り返します。ちなみにデカドロンの投与法は原法の投与法ではなく、多くの施設で広く行われている第1日目~第4日目のみの1日2回点滴を採用しています。
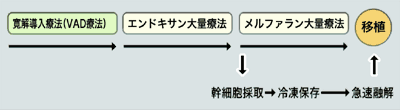
VAD療法で寛解導入をしたあと、引き続きエンドキサン大量療法、自家末梢血幹細胞採取・凍結保存を行います。メルファラン大量療法後に自家末梢血細胞移植を行うというのが初回治療の流れとなります。

*7 VAD療法の副作用(毒性)
一般に化学療法後には、吐き気、嘔吐、食欲低下などの消化器症状や脱毛、一時的な白血球や血小板の減少、あるいは貧血といった骨髄抑制が認められます。オンコビンの副作用として手足のしびれ、便秘などの末梢神経障害、アドリアシンの副作用として心筋障害、デカドロンの副作用として高血圧、高血糖、胃潰瘍、易感染性、食欲亢進、不眠、骨粗鬆症などがあります。もっとも注意が必要なのは白血球減少時の感染症です。しかし、専門医が注意深く行えば、生命にかかわるような重篤な副作用がおこることはまれです。


