進行別 がん標準治療 神経膠腫は、できるだけ多くの腫瘍を取り、放射線と抗がん剤の併用療法が基本
再発を防ぐ放射線と化学療法の併用
●術後補助療法
手術で残ったがん細胞を叩き、再発を防ぐのが術後補助療法です。これにも腫瘍をできるだけゼロに近づける寛解導入療法とその状態を維持するための維持療法があります。
・寛解導入療法
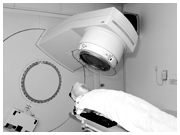
脳腫瘍に対するリニアックを用いた放射線治療
アメリカでは、化学療法単独、放射線単独、あるいは両者の併用でも術後補助療法を行ったほうが、手術単独で治療するより生存期間が延びることが証明されています。
日本では基本的には、放射線治療と抗がん剤による化学療法が併用されています。長島さんによると「放射線治療は、リニアックによるX線の多分割外照射で、局所照射がスタンダード」といいます。つまり、何回にも分けて毎日少しずつ外から病巣部に絞って放射線を照射します。脳全体に照射する全脳照射は副作用が大きく、現在では行われなくなっているそうです。入院して1日1.5~2グレイずつ週5日間、計60グレイ前後を照射するのが標準的です。
しかし、これでもまだ十分とは言えません。100グラム、つまり10の11乗個の脳腫瘍を手術で99パーセント、さらに放射線で99パーセント叩いたとしても、まだ10の7乗個のがん細胞が残る計算になるからです。これを化学療法でさらに叩こうというわけです。現在は、放射線との相乗効果を狙って、放射線治療と一緒に化学療法を行うのが一般的です。
ただし、化学療法に関しては「わが国ではまだ確立された標準治療はなく、ニトロソウレア系抗がん剤のニドラン(一般名ニムスチン=ACNU)を中心にして、さまざまな治療が行われているのが現状」と長島さんは語っています。
ニドランが基本になっているのは、前述の術後補助療法に関するアメリカの臨床試験が根拠になっています。ここで使われたのは同じニトロソウレア系のBCNU(一般名カルムジン)という抗がん剤でした。日本ではBCNUが認可されていないため、日本で独自に開発されたニドランが基本になっているわけです。
ニドラン単独がいいのか、多剤併用がいいのか、これもまだ十分な検証は行われていません。しかし、日本ではニドランを基本にIFN-β(一般名インターフェロンベータ)あるいはオンコビ���(一般名ビンクリスチン)やブリプラチン(もしくはランダ、一般名シスプラチン)などを併用することが多くなっています。こうした組み合わせや使い方、投与量などを考えると、「日本ではニドランを基本にして、それぞれの施設で独自の治療が行われているのが現状」だそうです。
| 種類 | 薬剤名 | BBB通過 | 適応症 | |
|---|---|---|---|---|
| アルキル化剤 | ナイトロジェンマスタード系 ニトロソウレア系 | エンドキサン(シクロホスファミド) ニドラン(ACNU) サイメリン(MCNU) | - ++ ++ | 悪性リンパ腫 神経腫瘍 脳腫瘍 悪性リンパ腫 膠芽腫 悪性リンパ腫 |
| 代 謝 拮 抗 薬 | フルオロウラシル誘導体 葉酸拮抗物質 サイトシンアラビノシド誘導体 | 5-FU(フルオロウラシル) フトラフール(テガフール) メソトレキセート(メトトレキサート) キロサイド(シタラビン) | ++ ++ - - | 頭頸部腫瘍 頭頸部がん 白血病 悪性リンパ腫の 中枢神経系への 転移 |
| 植物アルカロイド | ビンカアルカロイド ポドフィロトキシン | オンコビン(ビンクリスチン) ラステット・ベプシド(エトポシド) | + + | 神経芽腫 悪性リンパ腫 悪性リンパ腫 |
| 抗生物質 | BLM(ビノマイシン) | - | 悪性リンパ腫 頭頸部がん | |
| その他 | ナツラン(プロカルバジン) ブリプラチン(シスプラチン) パラプラチン(カルボプラチン) IFN-β(インターフェロン-β) | ++ - - - | 悪性リンパ腫 神経芽細胞腫 頭頸部がん 悪性リンパ腫 頭頸部がん 膠芽腫 髄芽腫 星細胞腫 | |
・維持療法
寛解導入療法によって腫瘍が減少した状態を維持するために行われる化学療法です。
維持療法の有効性を証明する科学的な根拠はまだありませんが、現在、専門医のほとんどが実施しています。長島さんは、「2年間ぐらい維持療法を続けますが、予後がいいという印象があります」と語っています。もっとも、2年間維持療法を続けられる人は、もともと状態がいい人が多いのです。長島さんは、ニドランを3カ月に1回の割で投与、またはIFN-βを2週間に1回の割で投与して維持療法としていますが、その使用量や投与間隔は施設によって異なるそうです。
現在、こうした術後補助療法に関しても、その有効性や治療法の標準を明らかにするために国内で臨床試験がスタートしています。
抗がん剤と脳腫瘍
最近、分子標的治療薬をはじめ、他の部位のがんに関しては新薬の開発が進んでいます。これに比べると、脳腫瘍は化学療法の進歩がもうひとつ停滞している感があります。
これは、ひとつには脳腫瘍の特殊性にあります。脳は、重要な臓器であるため、血液中の物質が簡単には脳内に進入できない仕組みになっています。これが、「血液脳関門」(ブラッド・ブレイン・バリア=BBB)です。この関門があるため、脳腫瘍に到達できる抗がん剤はACNUやビンクリスチンなどごく限られているのです。
そこで、最近はこの関門を強行突破する方法も研究されています。たとえば、アメリカでは一部でマニトールという薬を一気に大量注入して、血液脳関門を開かせて抗がん剤を投与する方法が行われました。この方法だと全身にケイレンが起きるので、全身麻酔をして行われますが、一般的ではありません。
脳腫瘍に流れ込む動脈に直接抗がん剤を注入する方法も研究されましたが、これは効果はあまり高まらず、逆に副作用が高まるため、欧米の大規模臨床試験で否定されています。髄腔内に広がった脳腫瘍に関しては、髄空内に直接抗がん剤を投与する方法がありますが、まだ十分な効果は立証されていません。
一方、最近テモダール(一般名テモゾロマイド)という新薬の臨床試験が行われています。これは飲み薬であることが特徴で、退形成星細胞腫や膠芽腫などに効果が期待されています。
化学療法が効果を発揮する乏突起膠腫
●乏突起膠腫
星細胞と同じように脳神経細胞を支える乏突起細胞から発生した腫瘍です。したがって、神経膠腫の一つに分類されますが、悪性度はそれほど高くなく、グレード2に入ります。
乏突起膠腫は、最近化学療法が効果があることがわかり、治療の標準化が進みつつあります。再発した悪性乏突起膠腫の人に化学療法を行った結果、高い奏効率(縮小効果)が得られることがわかったのです。これは、PCV療法といって、ナツラン(一般名プロカルバジン)とCCNU(一般名ロムスチン)、オンコビン(ビンクリスチン)という3種の抗がん剤を併用する方法です。この組み合わせは、初発、再発を含めて75パーセントという高い奏効率が得られたという報告もあります。その後、悪性のみならず通常の乏突起膠腫にも有効であることがわかりました。
遺伝子レベルでみると、乏突起膠腫は1番と19番の染色体に異常(LOH)が高率に認められ、こうした異常があるとPCV療法が有効に働き、明らかに生存期間が長いことが認められています。
そこで、世界ではPCV療法が標準になりつつあります。日本の場合、CCNUが認可されていないのでニドランを代わりに使っていますが「切れ味はいい」と長島さんは語っています。こうした治療で、2年生存率は85~90パーセントに上昇しており、最近ではPCV療法で再発がないというデータも出てきているそうです。
●悪性リンパ腫
ふつう悪性リンパ腫といえば、体のリンパ節などリンパ組織に発生するものです。本来脳にはリンパ組織は存在しないはずなのですが、頭蓋内に発生する悪性リンパ腫があります。エイズや免疫抑制剤によって著しく免疫が低下している人に発生する傾向がありますが、そうでない例も増えています。多くは脳実質にしみ込んで広がっていく悪性の脳腫瘍です。
ふつう悪性リンパ腫は、T細胞というリンパ球ががん化したものですが、脳の悪性リンパ腫はB細胞から発生したものが多いことが特徴です。体に発生する悪性リンパ腫に有効な化学療法は全く効果がありません。したがって、これまで第一選択は放射線治療とされてきました。ただし、放射線でいったんは腫瘍が消失しても、90パーセントは短期間に再発します。これが問題だったのです。
ところが、最近になってメソトレキセート(一般名メトトレキサート)という抗がん剤の大量投与が有効であることがわかってきました。ただし、放射線と併用するととくに高齢者で高率に白質脳症が起こり、痴呆状態になる危険があります。しかし、高齢者の場合メソトレキセートの大量投与だけで、放射線を併用した場合と治療効果は同等で、かつ白質脳症などが少ないと報告されています。そこで「おそらく今後は、メソトレキセートの大量投与が第一選択となり、再発したら放射線となっていくのではないでしょうか」と長島さんは見ています。
手術による摘出には治療的意味合いはほとんどなく、組織の確認にとどまります。
同じカテゴリーの最新記事
- 手術技術、化学療法、遺伝子診断、そしてチーム医療が重要 治療成績が向上する小児脳腫瘍
- ウイルス療法が脳腫瘍で最も悪性の膠芽腫で高い治療効果! 一刻も早いウイルス製薬の量産化技術確立を
- 悪性脳腫瘍に対する緩和ケアの現状とACP 国内での変化と海外比較から考える
- 脳腫瘍グレードⅣの膠芽腫治療に光射す 標準治療に自家腫瘍ワクチン療法を加えて生存期間延長を目指す
- 他のがん種よりも早期介入が必要 目を逸らさずに知っておきたい悪性脳腫瘍の緩和・終末期ケア
- 新たにウイルス療法や免疫チェックポイント阻害薬など 悪性度の高い膠芽腫などの脳腫瘍治療に見えてきた可能性
- 光の力でがん細胞を叩く治療 悪性脳腫瘍に光線力学的療法(PDT)併用の実力
- 標準治療では治癒が難しい悪性脳腫瘍の治療に光明が ホウ素中性子捕捉療法「BNCT」の実用化が見えてきた
- 脳転移治療にはガンマナイフが効果的 さらに患者にやさしい新型登場


