分子標的薬と抗がん剤併用による大腸がん休眠療法 何を投与するかよりも、どのくらいの量を投与するかが決めて
分子標的薬を主にした併用
| 分子標的薬 | 従来の抗がん剤 | |
|---|---|---|
| 標的 | 増殖に関わる分子 | 分裂、増殖 |
| 毒性 | 軽い | 重い |
| 縮小効果 | 小さい | 大きい |
| 継続性 | 長期間 | 短期間 |
| 耐性 | 起こりにくい | 起こりやすい |
| 戦略 | 長期戦 | 短期決戦 |
では、このような分子標的薬を使って、他のがんでもGISTと同じように増殖を抑え、延命させることができるかというと、実はそうはいかない。
「GISTでは増殖に関与する遺伝子が1個だけで、それを標的にしたためにそれができたのですが、他のがんではそういう遺伝子が5個も6個もあり、なおかつ人によって異なっている可能性があるので、おそらく100個以上の分子標的薬を用意しないと実現できないと思います。そこで、当分の間は、分子標的薬と抗がん剤を併用する必要がありますが、その際、大事なことは、分子標的薬を中心にして抗がん剤を併用することです」
最近、次々に新しい分子標的薬が出てきているが、その使用のほとんどは抗がん剤との併用である。しかも、その場合、あくまでも抗がん剤が主体で、分子標的薬は従の関係の併用である。冒頭のアバスチンの場合も、抗がん剤との併用効果が認められて標準治療薬になっているが、その場合もFOLFOX(5-FU、ロイコボリン、オキサリプラチン併用)という抗がん剤が主体で、それにアバスチンが併用されているにすぎない。しかし、高橋さんは、同じ併用療法でも抗がん剤と分子標的薬のどちらを主体にするかで、治療が根本的に変わってくるという。
ボトル1本飲ませる治療
「現在の抗がん剤治療は、がんを縮小するのが第1のねらいで、そのためにがんをたたく力の強い、短期決戦型の抗がん剤を主体にし、それに分子標的薬を合わせるやり方です。その場合、抗がん剤は、最大耐用量と称して、ヒトが耐えられる限界量が投��されることになります。これは、たとえて言えば、アルコールを初めて飲む場合にウイスキーボトル1本の量から飲ませるようなものです」
もちろん、ボトル1本ぐらい平気な人もいようが、まったく飲めない下戸もいる。このように、アルコールの適量には人により個人差があるのに、誰に対してもボトル1本飲ませるのが、現在の抗がん剤治療のやり方だという。これは、誰が考えてもムチャクチャなやり方のように思うが、これが抗がん剤の世界では、がんの縮小という目標のために許されてきたというのだ。
しかし、そのために、患者は副作用で苦しい思いを余儀なくされる。この副作用がひどくなりすぎると、そこで治療は中止となり、打つ手がなくなり、治療を求めて彷徨うがん難民を生み出すことになる。そこで、高橋さんは、併用の主体を抗がん剤から分子標的薬に切り替え、治療を根本的に変える必要があるというのだ。
「分子標的薬は、治療を長く継続することにより効果が現れる薬で、いわば長期戦型です。従来の抗がん剤とは性格が全然違う。この分子標的薬を主体にし、がんの縮小を目標にせず、長く継続させる治療に切り替える必要があります。そして慢性疾患のように、がんをマネージすることができれば、延命ができます。ただし、治療が継続できるかどうかは、抗がん剤の投与量で決まるのです」
副作用の出方で増減する治療
そのためには、当然ながら、抗がん剤をボトル1本から始めるのではなく、もう少し少ない量からスタートしなくてはならない。ここで重要なのは、アルコール同様、抗がん剤の適量にも個人差が相当にあるということだ。薬剤によって異なるが、5倍から50倍も異なるとの報告もある。これほど大きな個人差に対して、薬剤の投与量を一律にするのは理に合わない。そこで、最初は一律の量からスタートしても、それ以後は患者の副作用の出方に応じて薬剤の投与量を増やしたり減らしたりしていき、その人に合った一番の適量を見つけていく。
高橋さんは、この治療の方法論を編み出した。名づけて、「個別化最大継続可能量」による抗がん剤治療といい、これが休眠療法の具体案である。
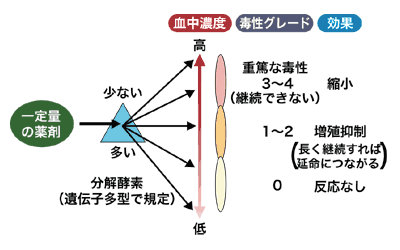
「具体的には、あらかじめ抗がん剤投与の最大量(現在の標準的投与量)と最低量(最小有効濃度)を決め、その中央あたりから増減していく。その増減の指標として、毒性(副作用)の強さで量り、グレード1か2になるようにしていくのがこの治療です。グレード2までなら治療を継続できます」
グレード2といえば、最悪の日で下痢が4~6回起こり、嘔吐が2~5回増加する程度で、患者にとってはこれでもつらいものだが、それでも治療の継続は可能だという。
たとえば、大腸がんでもよく使われるイリノテカン(商品名はカンプトやトポテシン)の場合なら、標準的な投与量は体表面積あたり125ミリグラム(TS-1併用時)、最小有効濃度はこれまでの報告から25ミリグラムなので、その中央の75ミリグラムから治療を開始。その結果、副作用のグレードが2なら次回も同量で治療を行い、グレード1か0なら25ミリグラム上げて100ミリグラムに増量、グレード3か4なら逆に50ミリグラムに減量、というように投与量を変えていき、最終的にその人の適量を見つけ、その量で治療を継続していくというわけだ(すでに全国的な臨床試験が終了)。
毒性を指標とする根拠は、抗がん剤の血中濃度と毒性が相関することにある。つまり、この治療は個々の患者の血中濃度が等しくなることを目標としている。
[抗がん剤の毒性(副作用)のグレード表]
| 0 | 1 | 2 | 3 | 4 | |
|---|---|---|---|---|---|
| 白血球 (×10/μL) | 3.3-8.8 | <3.3-3.0 | ≧2.0-<3.0 | ≧1.0-<2.0 | <1.0 |
| 血小板 (×10/μL) | 130-350 | <130-75 | ≧50-<75 | ≧10-<50 | <1.0 |
| ヘモグロビン (g/dL) | 13.5-17.5 | <13.5-10.0 | 8.0-<10.0 | 6.5-<8.0 | <6.5 |
| 嘔吐 | なし | 治療前に比べ、1日当たり1回多い | 治療前に比べ、1日当たり2~5回多い | 治療前に比べ、1日当たり6回以上多い。または静注補液が必要 | 集中治療を要する生理機能状態 |
| 下痢 | なし | 治療前に比べ、<4回/日の排便回数増加 | 治療前に比べ、4~6回/日の排便回数増加、または夜間排便 | 治療前に比べ、≧7回/日の排便回数増加、または失禁、脱水に対する輸液を必要とする | 集中治療を要する生理機能状態、または循環動態の虚脱 |
| 脱毛 | なし | 軽度(枕につく) | 著しい脱毛 | - | - |
同じカテゴリーの最新記事
- 切除可能な直腸がん試験結果に世界が注目も 日本の標準治療は「手術」で変わりなし
- ビタミンDの驚くべき効果がわかってきた 消化管がん手術後の再発・死亡リスクを大幅に減少
- 世界最大規模の画期的研究の一部解析結果が発表 大腸がんの術後補助療法の必要性をctDNAで判断する
- 初めての前向き試験で抗EGFR抗体薬の信頼性が確実に! 進化を続ける切除不能・進行再発大腸がんの薬物療法
- 遺伝子変異と左右どちら側にがんがあるかが、薬剤選択の鍵を握る! 大腸がん薬物療法最前線
- 化学放射線と全身化学療法を術前に行うTNT療法が話題 進行下部直腸がん 手術しないで完治の可能性も!
- 肛門温存の期待高まる最新手術 下部直腸がんTaTME(経肛門的直腸間膜切除術)とは
- 大腸のAI内視鏡画像診断が進化中! 大腸がん診断がより確実に
- 患者さんによりやさしいロボット手術も登場 新しくなった大腸がんの手術と薬物療法


