手術やラジオ波治療ができなくてもあきらめない 難治性の肝細胞がんに対するナノナイフ治療(IRE)
治療効果はエコーを確認して
では、治療が有効だったかどうかは、どのように判断するのだろうか。
「ナノナイフの治療効果が良好な場合、がん細胞の血流がなくなります。治療終了前にそれを確認することで、適切に治療ができたかどうかの判断をしています。これはラジオ波やマイクロ波による治療でも同様です」
その確認の方法は、放射線科医はCTの画像で評価をするのが一般的だが、杉本さんら内科医は超音波(エコー)に慣れているため、造影剤を使ったエコー検査を行っているそうだ。
「理由は、造影剤を使ったエコーのほうが造影剤を使ったCTよりも血流を検出する感度が高いためです。ときにエコーの画像では明瞭に見えないがんがありますが、最近は、『フュージョン・イメージング』という手法を用いて、安全かつ効果的な治療を行うようにしています。これは過去に撮影したCTやMRIの画像を、超音波の画面に同期させ表示するシステムです。
とくに、ナノナイフでは複数の針をがんの内部や周囲に正確に配置する必要があります。フュージョンでCTやMRIの針C面(穿刺ラインに直交する断面)を表示することで、3次元的な認識が良好になり、より正確な治療が行えます」(画像6)
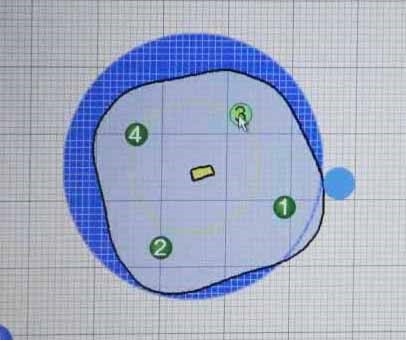
「また、ナノナイフ治療は全身麻酔で行うため、ラジオ波のように残存部位を翌週に再度治療するということが気軽にできません。ですから、画像上がんが残っている疑いがあるときにはその場で追加治療を行い、可能な限り1回の治療で終えるようにしています」
体へのダメージの少ないナノナイフ治療だが、技術的には一定の習得が必要なようだ。例えば、電流を均等に効果的に流すためには、針と針を平行に均等に刺す技術がいるという。
「技術習得は必要ですが、ある程度経験を積めば問題なくできます。むしろフュージョン・イメージングのような治療支援のシステムの確立が大事だと思います」と杉本さん(画像7)。
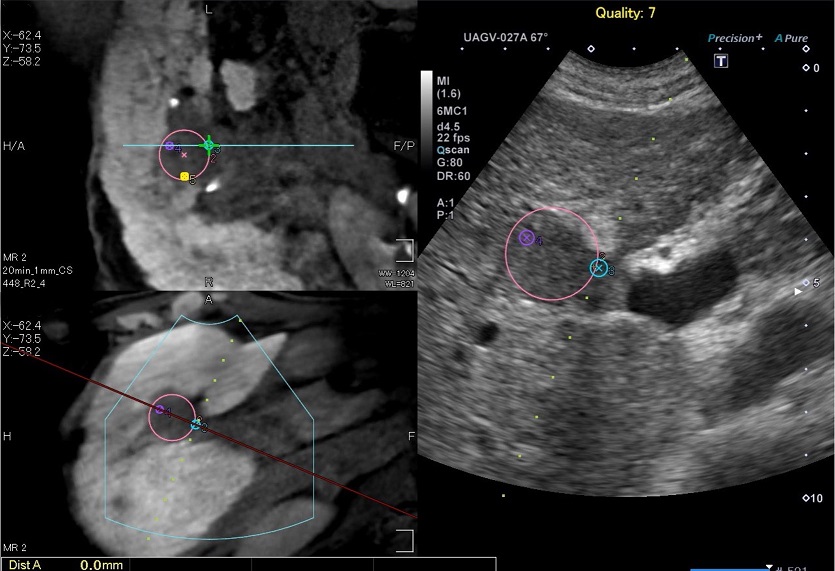
治療1年あまり、治療箇所に再発なし
これまで何例くらいの患者さんに行い、どんな効果が出ているのだろうか。
「先進医療の承認を得る前に約30例(肝細胞がん、転移性肝がん、膵がんを含む)、得たあと7例(肝細胞がんのみ)行いました。まだ1年という途中経過ですが、治療を行った箇所に今のところ再発は見られません。もちろん、今後は長期的な予後を調査する必要があります。また、入院期間の延長や、処置が必要な合併症は経験していません。ですから、手術やラジオ波などができない患者さんにとっては、非常にいい選択肢の1つだと思います」
今後はどのように進めて行くのだろうか。
「承認をめざすためには、多施設に治療が拡がる必要があります。現在は標準治療が困難な難治性の肝細胞がんだけが対象になっていますし、治療機器も高価で、なかなか広がる状況にありません。欧米では広く行われている治療なので、これはとても残念なことです。
今行っている臨床試験はナノナイフ治療単独の試験であり、他の治療法との比較試験は行えていません。本来であれば、ラジオ波が困難ながんに対する標準治療である肝動脈塞栓術や放射線治療との比較試験を行い、ナノナイフ治療の優位性が示せればいいのですが、今のところ過去の治療と比べて遜色がないというところまではいえる段階です。しかし、将来的には保険収載を目標に、これらの比較試験を行って行きたいと考えています」と杉本さんは語る。
海外で先行するナノナイフ併用試験にも期待
がん種は違うが、膵がんにおいて、ステージⅢの局所進行膵がんの患者さんを対象にした「DIRECT試験」が米国で走り始めたのだ。1つは膵がんの標準治療である「FOLFILINOX治療単独」vs.「FOLFILINOX+ナノナイフ治療」の多施設共同無作為化比較試験。もう1つは「別な抗がん薬単独」vs.「抗がん薬+ナノナイフ治療」を比較した観察登録試験だ。
「膵がんは最近増えていますし、なかなか有効な治療法がないので、保険適用される可能性はあると思います。これが突破口になればいいと思いますね」
もう1つトピックがある。ナノナイフによる治療の結果、死んだがん細胞を貪食したマクロファージが、ほかの免疫細胞に「同じがん細胞をやっつけろ」という情報を伝達することで、離れた箇所にある未治療のがんも縮小させる効果があるというのだ。
「アブスコパル効果といいますが、もともと放射線治療において唱えられ始めた理論です。ナノナイフでも可能性があるかもしれないと思うのは、放射線治療もナノナイフ治療もがんを徐々にアポトーシスに導くという点で共通しているためです」
また、杉本さんはナノナイフの〝がん微小環境のリセット〟という視点からも可能性をみている。
「がんは、免疫の監視から逃避するように働きかけています。そこで、がんにナノナイフを行うことでこれら負のがん微小環境をリセットし、免疫細胞がより攻撃しやすい環境を作り出せればと思います。そのため、がんが免疫から逃れるシステムをブロックしてがんを死滅させる免疫チェックポイント阻害薬との併用療法が、今後はむしろ期待できるのではないかと思います。
日本でも昨年(2020年)9月、肝がんに対して免疫チェックポイント阻害薬のテセントリク(一般名アテゾリズマブ)が保険適応されましたが、すでに免疫チェックポイント阻害薬オプジーボ(一般名ニボルマブ)+ナノナイフ治療の多施設第Ⅱ相試験(NCT03630640)がフランスでは始まっていると聞いています」
最後に、杉本さんは今後の見通しを語ってくれた。
「すべての施設にナノナイフ治療機器がある必要はなく、もしも原発性の肝細胞がんで、『手術できない』『ラジオ波焼灼療法はむずかしい』といった診断を受けたときは、当院を中心としたいくつかのhigh volumeセンターで治療が受けられるようになればいいと思います。また、今後肝細胞がんの治療に免疫チェックポイント阻害薬の重要性がより増してくると思われます。ナノナイフの腫瘍免疫効果を検証し、将来的に臨床応用できればと考えています」
同じカテゴリーの最新記事
- 免疫チェックポイント阻害薬の2剤併用療法が登場 肝細胞がんの最新動向と薬物療法最前線
- 肝がんだけでなく肺・腎臓・骨のがんも保険治療できる 体への負担が少なく抗腫瘍効果が高いラジオ波焼灼術
- 高齢の肝細胞がん患者さんに朗報! 陽子線治療の有効性が示された
- 手術やラジオ波治療ができなくてもあきらめない 難治性の肝細胞がんに対するナノナイフ治療(IRE)
- 高い治療効果が期待できる 切除不能・進行肝細胞がんの最新化学療法
- ラジオ波の利点はがんをくり抜き、何度でも 再発進行肝細胞がんと転移性肝がんの治療にもラジオ波焼灼療法が有望
- 治療選択の拡がりが期待される 肝細胞がんの1次治療に、約9年ぶりに新薬登場!
- 進行肝がんに対するネクサバールのマネジメント
- 手術ができれば根治も!肝内胆管がんの治療法


