- ホーム >
- 薬 >
- 免疫チェックポイント阻害薬
エビデンスとともに適応拡大へ 免疫チェックポイント阻害薬
肺がんなどにも効果あり 日本でも適応拡大の方向
米国では、オプジーボは多くのがん種で有効性が示されており、15年3月に非小細胞肺がん(NSCLC)の扁平上皮タイプで承認された。また、非扁平上皮タイプにおいても第Ⅲ(III)相試験での治療成績が途中経過において*タキソテールを明らかに上回っていたことから試験が途中で打ち切られ、年明けには非小細胞肺がん全体への適応が承認される見込みだ。日本でも肺がんに対する適応の申請が行われている。早めの承認がなされる可能性が高い。
「今後の適応拡大の対象としては、腎細胞がん、膀胱がん、頭頸部がん、胃がん、食道がん、卵巣がんなどの既治療の進行がんにおいて、第Ⅲ(III)相臨床試験が施行あるいは準備されています。さらに早期試験レベルでは、ホジキンリンパ腫、非ホジキンリンパ腫、肝細胞がんなどで高い奏効率が示されています」
*タキソテール=一般名ドセタキセル
併用療法も有効 ASCOでも大きな注目
このように、日本に限らず全世界的に免疫チェックポイント阻害薬に対する医療関係者の注目度が増している。
「懐疑的だったものから、科学的に間違いなく効いているということに、臨床医、腫瘍内科医たちが手応えを感じています。学会での注目度が違います。今年の*ASCO2015では、免疫系の研究報告会場で満員が目立ちました」
注目されたのが、メモリアル・スローンケタリング・がんセンターの*ジェッド・ウォルチョック医師が報告した、進行悪性黒色腫患者を対象とした1次治療薬としてヤーボイとオプジーボの併用療法の第Ⅲ(III)相臨床試験「CheckMate067試験」の結果だった。
異なるチェックポイントに作用するヤーボイとオプジーボの複合免疫療法を評価した初の第Ⅲ(III)相試験で、患者945人が以下の3群に割り付けられた。❶ヤーボイ+オプジーボを4回併用投与後、オプジーボ単独で継続群❷オプジーボ+プラセボ(偽薬)群❸ヤーボイ+プラセボ群
結果は、無増悪生存期間(PFS)の中央値は、❶が11.5カ月、❷が6.9カ月、❸が2.9カ月で、併用群、オプジーボ群ともにヤーボイ群より効果があることが統計学的に示された。奏効率(ORR)でも同様な傾向が見られた。
*ASCO2015=2015年米国臨床腫瘍���会年次学術集会 *ジェッド・ウォルチョック医師(北野さん留学時代の直属の上司)
遅発性の効果も 免疫系の副作用に注意
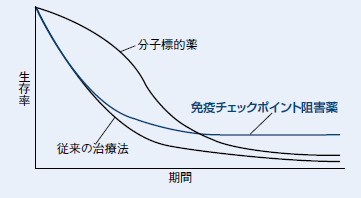
生存曲線の比較(イメージ)
免疫チェックポイント阻害薬が優れている点について、北野さんは「T細胞はいろいろな変異抗原を持つがん細胞を相手に戦っています。そこにかかってしまったブレーキを外しに行くのが免疫チェックポイント阻害薬ですが、理論上は抗原と戦っているT細胞だけを活性化させるので、他の細胞には関与しません」と語る。
効率も安全性もよいというわけだ。多くのケースでは投薬当初から効果が現れるが、一部の症例に限られるが、いったん腫瘍が大きくなった後で効果が出始めることがある。遅発性の効果という。生存曲線、無増悪生存曲線も特徴的で、分子標的薬などは上に凸のカーブになるが、免疫チェックポイント阻害薬は下に凸が現れる。効き始めはゆっくりで、ある一定のところでフラットになる(図3)。進行悪性黒色腫でヤーボイを使用した2割弱に10年ほどの長期生存を認めたとの報告も出てきた。
「まだ悪性黒色腫のデータだけですが、難治性がんで生存曲線が横ばいになるということは画期的なことです。今後は完治する患者さんも出てくるかもしれない。まだ歴史が浅い薬なので、他のがん種も含めた長期フォローの結果に注目しています」
心配されるのは、副作用。
「全く副作用のない治療はありません。がんを攻撃して正常細胞も犠牲になる抗がん薬とは作用機序が異なり、自己免疫に関わることなので、種類もタイミングも異なります。いままでに経験のない副作用が生じる傾向があり、今後の課題です」
日常生活に影響が出るグレード3の副作用が発現するのはヤーボイで約20%、オプジーボで10数%、米国で14年9月に承認された抗PD-1抗体*Keytruda(キイトルーダ)で10%未満。多いのは、肝障害、肺障害(肺炎など)、消化器障害(下痢、大腸炎など)。
その他、皮膚障害、内分泌系障害(甲状腺機能低下症、下垂体機能低下症、副腎機能低下症など)、神経系障害(重症筋無力症、眼障害、膵炎など)。このうち、下垂体機能低下症、重症筋無力症などは生命に関わることもある。副作用を早期発見して投薬を中止し、ステロイド薬で免疫を抑制すればほとんどの場合回復するが、自己免疫系の副作用は長期化する傾向もある。
*Keytruda(キイトルーダ)=一般名pembrolizumab(ペムブロリズマブ)
抗がん薬、分子標的薬との併用 遺伝子検査で効果予測も
ここ数年で大きな転機を迎えたがん免疫療法だが、これからはどのようなことが期待されるか。
「免疫チェックポイント阻害薬単剤での開発が複数のがん種で成功しつつある中、次の開発戦略としては併用療法が期待されます。同じような作用機序をもつ免疫療法の併用をはじめ、殺細胞性抗がん薬あるいは分子標的薬によりがん細胞を直接攻撃し、さらにがん免疫治療による攻撃で追い打ちをかけるという併用療法も臨床研究がなされています」
放射線治療も含めた併用療法の臨床試験は数百というレベルで行われているという。さらに免疫チェックポイント阻害薬が増えれば、併用療法の組み合わせも増えることになる。
「最近は、遺伝子変異の数が多いがんでは免疫系に異物と認識される抗原が発生しやすく、治療効果が高い傾向がある、との報告がなされていますが、免疫力には個体性があるので、個々の患者さん自身の免疫力の強さにより効果に差があることも忘れてはいけません。今後は遺伝子レベルでの免疫機能の解明が進み、がんの性質はもちろん宿主の免疫状態も含めてより包括的にがん免疫療法に適した人、そうでない人の予測ができる時代が来ることでしょう」
治療の中で、より効果的なケースで選択されるための研究が進んでいる。
同じカテゴリーの最新記事
- 免疫チェックポイント阻害薬との併用療法で大きく前進 新たな進行期分類が登場した子宮体がんの現在
- 免疫チェックポイント阻害薬で治療中、命に関わることもある副作用の心筋炎に注意を!
- キイトルーダ登場前の時代との比較データから確認 進行性尿路上皮がんの予後が大幅に延長!
- 肺がんに対する免疫チェックポイント阻害薬の治療効果は腸内細菌が関係!
- 複合がん免疫療法が、がん薬物療法の主力に! 免疫療法の個別化医療を目指す
- 胃がん新ガイドライン「条件付き承認」で増える治療選択 1次治療でオプジーボ承認
- 乳がん治療にも免疫チェックポイント阻害薬が登場! トリプルネガティブ乳がんで承認、さらに――
- 初期治療から免疫チェックポイント阻害薬選択の時代へ 腎細胞がん治療はここまで来た!
- 患者にもわかりやすく明確化された推奨する治療・しない治療 全面改訂された「大腸癌治療ガイドライン」2019年版


