- ホーム >
- 薬 >
- 免疫チェックポイント阻害薬
患者にもわかりやすく明確化された推奨する治療・しない治療 全面改訂された「大腸癌治療ガイドライン」2019年版
再発リスクに応じた治療選択を提示
近年、大腸がんに対する薬物療法の選択肢は飛躍的に増えたため、薬物療法に対する改訂も増えてきた。
「従来は〝化学療法〟という表現のカテゴリーでしたが、細胞障害性抗がん薬以外に、分子標的薬、免疫チェックポイント阻害薬などさまざまな性質の薬が出てきましたので、〝薬物療法〟という表現に変わりました」
術後補助化学療法は、経静脈で投与するエルプラット(一般名オキサリプラチン)併用療法が良いのか、あるいは経口薬のフッ化ピリミジン系薬剤の5-FU(同フルオロウラシル)、UFT(フルオロウラシルのプロドラッグ)、ゼローダ(同カペシタビン)などが良いのか侃侃諤諤(ケンケンガクガク)の議論だったという。
「従来はいずれも同等な推奨度だったのですが、日本は手術のクオリティが高く、再発リスクはそれほど高くないという見地から、わざわざ、強いエルプラットを投与する必要がないのではないかという外科医サイドの意見と、海外と同じように1次治療はエルプラット併用療法をやるべきだという腫瘍内科医サイドの意見がありました。そこで図2のようなグラフ(再発リスクに応じた治療選択)を示し、ローリスクはフッ化ピリミジン系、ハイリスクはエルプラット併用療法を推奨ということを提示しました」(図2)

エルプラットは副作用として神経症状が出て患者のQOL(生活の質)は下がるが、これをフッ化ピリミジン系のゼローダとの併用であるCAPEOXにすると、3カ月投与の場合では神経症状が少ないということがわかったという。
切除不能の進行がんに対する薬物療法も、大腸がんではかなりの進歩が見られる。
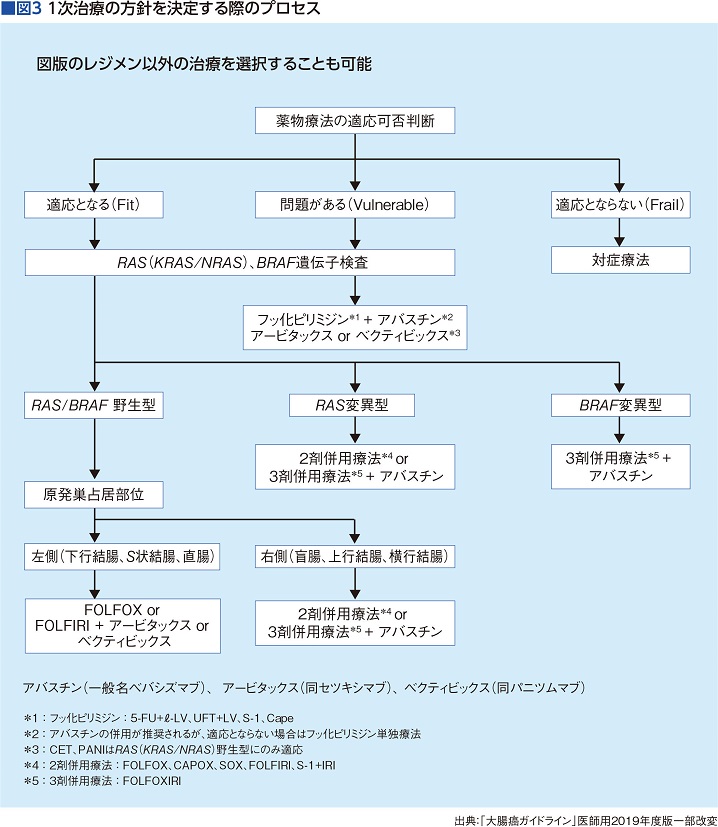
「進行がんに対する薬物療法は延命が目的になりますから、生命予後と同時に日常生活における副作用の影響が患者さんにとっては重要です。1次治療はかなりの選択肢があり、腫瘍内科の専門医でない限り、選択に迷うケースもあります。そこで今回の改訂では、図3(1次治療の方針を決定する際のプロセス)のように整理して提示しました。患者さんの元気さ(PS:パフォーマンスステータス)や遺伝子変異マーカー、そして原発巣が左側(下行結腸がん、S状結腸がん、直腸がん)か、右側(盲腸がん、上行結腸がん、横行結腸がん)かによって投与を考慮しています」(図3)
1次治療の主要なレジメンは、抗がん薬と分子標的薬3種類のどれかだ。
免疫チェックポイント阻害薬は2次治療からも使えるように
今後は、大腸がんでは5%程度の患者が適応になる免疫チェックポイント阻害薬の投与についても重要なテーマだ。どのタイミングで投与するかという点がとくに重要だ。
「わずか約5%とはいうものの、適応する患者さんにとっては、比較的高い確率で長期の延命効果があるので福音となります。現在、標準治療がなくなった場合に投与できるというのがコンセンサスですが、大腸がんの場合、治療が豊富ですので、3次治療、4次治療まで治療を行えます。しかし、そこまで治療を行うと患者さんは衰弱してしまうかもしれず、せっかくの治療のチャンスを逸してしまう可能性があります。そこで、主治医が判断して、免疫チェックポイント阻害薬は2次治療からでも投与できるアルゴリズムとしました」
現在、大腸がんに対する免疫チェックポイント阻害薬は、キイトルーダ(一般名ペムブロリズマブ)とオプジーボ(同ニボルマブ)が適応となっている。
「ただし、免疫チェックポイント阻害薬には問題点もあります。というのも、免疫チェックポイント阻害薬が適応となる、MSI-Hの患者さんには、家系内にがんが多発するリンチ症候群の方が多く含まれています。遺伝子変異を調べることでリンチ症候群であることがわかると、患者さんご本人のみならず、お子さんなど血縁者の問題が生じてきます。その場合、どう伝え、対処していくのか、今後は遺伝子カウンセリングなどの対応も含めしっかりと対処する必要が出てきます」
その点については「遺伝性大腸癌ガイドライン」に詳しく記載される。
いずれにせよ、今回の「大腸癌治療診療ガイドライン2019」の改訂は、今後の大腸がんの診断・治療の指針として、大きく貢献し、さらに今後の課題を見据えることのできる意義のある改訂であると言えるだろう。
同じカテゴリーの最新記事
- 免疫チェックポイント阻害薬との併用療法で大きく前進 新たな進行期分類が登場した子宮体がんの現在
- 免疫チェックポイント阻害薬で治療中、命に関わることもある副作用の心筋炎に注意を!
- キイトルーダ登場前の時代との比較データから確認 進行性尿路上皮がんの予後が大幅に延長!
- 肺がんに対する免疫チェックポイント阻害薬の治療効果は腸内細菌が関係!
- 複合がん免疫療法が、がん薬物療法の主力に! 免疫療法の個別化医療を目指す
- 胃がん新ガイドライン「条件付き承認」で増える治療選択 1次治療でオプジーボ承認
- 乳がん治療にも免疫チェックポイント阻害薬が登場! トリプルネガティブ乳がんで承認、さらに――
- 初期治療から免疫チェックポイント阻害薬選択の時代へ 腎細胞がん治療はここまで来た!
- 患者にもわかりやすく明確化された推奨する治療・しない治療 全面改訂された「大腸癌治療ガイドライン」2019年版


