分子標的薬使用にあたっての RAS遺伝子野生型の重要性
RAS遺伝子野生型で治療効果 抗EGFR抗体薬
1次、2次治療で*アバスチンや抗EGFR抗体などの分子標的薬(表1)が適応となる症例には化学療法との併用が推奨されています。分子標的薬が適応とならない場合は化学療法単独が推奨されています。
もう1つ重要なことは、*アービタックスと*ベクティビックスはKRAS遺伝子の野生型にのみ適応されるということです。大腸がんにおけるKRAS遺伝子については、ここ数年話題となっていますが、特に昨年(2013年)相次いで、大規模試験の遺伝子解析データが報告され、KRASだけではなく、NRASなどRASファミリーと呼ばれる全RAS遺伝子の変異の有無により、治療効果に有意差のあること(野生型で無増悪生存期間、全生存期間に改善効果を認める)が報告され、大腸がん領域で最も大きなトピックスとなっています。
このように、分子標的薬の登場により、切除不能・進行再発大腸がんに対する治療環境は大きく変化し、治療の選択肢の幅が広がるとともに、個々の患者さんにも治療選択の権限が与えられるようになってきています。
その一方で、これらの治療法の選択や患者さんへの対応には医療側でのより専門的な知識や経験を要する時代になってきているとも言えそうです。
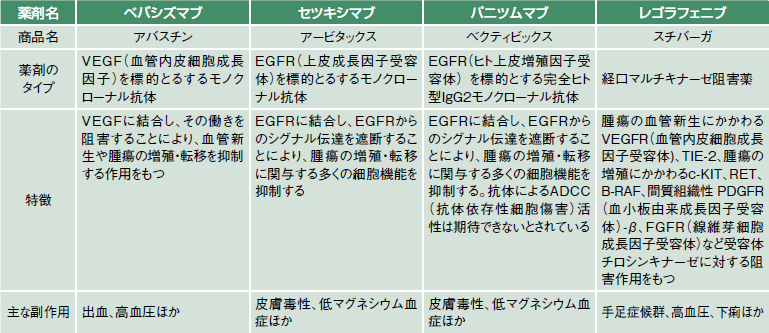
*アバスチン=一般名ベバシズマブ *アービタックス=一般名セツキシマブ
*ベクティビックス=一般名パニツムマブ
RAS遺伝子野生型の重要性
化学療法対象の切除不能・再発大腸がん患者における既治療例におけるRAS遺伝子変異型は約4割に上り、このような変異型症例に対しては、アービタックスやベクティビックスなどの抗EGFR(上皮成長因子受容体)抗体薬の有効性が認められないことが報告されています。RAS遺伝子には、KRAS、NRAS、HRASの3種類があり、これらはRASファミリーと呼ばれています。
RAS遺伝子を構成するRASタンパクはEGFRなどからの刺激を受けて活性型になり、下流への複数のシグナル経路を活性化させる役割をもっています。役割を果たしたあとは不活性型に戻ります。このRAS遺伝子に変異が生じると、常に下流にシグナルを送り続けることになり、この���とが発がんやがんの増殖に関与しているとされています。
2008年以降、国際学会や論文で、抗EGFR抗体薬の効果と、RASファミリーの1つKRAS遺伝子変異(エクソン2と呼ばれる部位)との関連が報告され始めます。腫瘍のKRAS遺伝子変異は抗EGFR抗体薬の負の効果(有効性が認められない)予測因子となるというものです(表2)。これらの報告に基づいて、抗EGFR抗体薬の投与前にKRAS遺伝子変異を測定し、効果予測すると患者さんの治療選択に有益であるという考えが出てきました。
さらに2013年4月以降、別の臨床試験や既存の臨床試験を詳細に検討した結果、KRAS遺伝子の別の部位の変異やNRAS遺伝子変異の認められる症例では、有効性が認められないことが明らかになってきました。このため欧米では従来、治療対象を「KRAS野生型」としていたものを「KRAS/NRAS野生型」とし、変異を認める症例にはガイドラインや添付文書で抗EGFR抗体薬の投与を推奨していません。
日本では、2011年にKRAS遺伝子変異検査が保険適用となり、普及していますが、NRASを含むRAS遺伝子変異の測定は現時点では保険適用となっていないため、「大腸癌治療ガイドライン2014年版」では、治療対象はまだ「KRAS野生型」となっています。
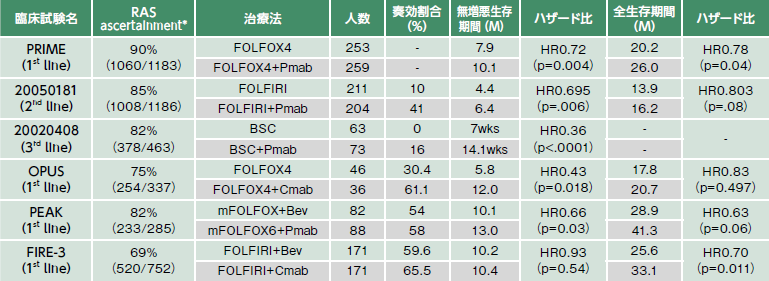
●Cmab:アービタックス=一般名セツキシマブ
●Bev:アバスチン=一般名ベバシズマブ
*RAS ascertainment:ランダム化された症例のうちRAS遺伝子変異の評価が可能であった症例の割合
出典:『大腸がん患者における RAS遺伝子(KRAS/NRAS遺伝子)変異の測定に関するガイダンス パブリックコメント用 第2版 2014年3月日本臨床腫瘍学会 』より
同じカテゴリーの最新記事
- 手術後の再発予防に加え、Ⅲ期の放射線化学療法後にも EGFR変異陽性肺がんタグリッソの治療対象さらに広がる!
- 有効な分子標的薬がなかったEGFRエクソン20挿入変異陽性肺がんに ついに承認された二重特異性抗体薬ライブリバント
- 世界に先駆け初承認された分子標的薬ロズリートレクの課題 共通の遺伝子変異を標的とする臓器横断的がん治療薬
- 進行・再発卵巣がんに選択肢が増える 初回治療から分子標的薬リムパーザが使える!
- 肺がんに4つ目の免疫チェックポイント阻害薬「イミフィンジ」登場! これからの肺がん治療は免疫療法が主役になる
- 肺がん薬物療法最前線―― 分子標的薬と、オプジーボに代表される免疫チェックポイント阻害薬が、肺がん治療をここまで変えた!
- 第3世代タグリッソ登場で非小細胞肺がん治療はさらに進化
- 分子標的薬投入時期を「Window」で見える化 ホルモン陽性HER2陰性再発転移症例での適切な投与時期を示唆
- 非小細胞肺がん 耐性後は再生検を行い 適切なEGFR-TKIで治療する
- 深い寛解後に 70%が投薬中止可能~慢性骨髄性白血病の治療~


