非小細胞肺がん 耐性後は再生検を行い 適切なEGFR-TKIで治療する
安全に細胞を採取できることが 再生検法を選択するポイント
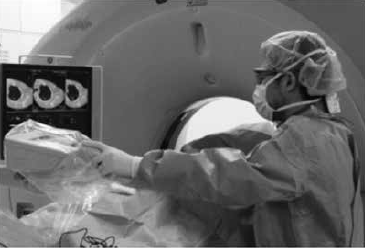
再生検の検体をどこから取るかについては、経気管支肺生検、CTガイド下肺生検などの方法により、原発巣、転移巣、胸水、腹水、髄液などがある(写真4)。検体として適した部位からの採取を選ぶというよりも、実際は、とにかく安全に採取できる部位が何とか1カ所でもあればまだ良いほうだという。
再生検が困難な場合もある。例えば、呼吸不全を伴う重症肺気腫併存症例、出血あるいは凝固異常があり気管支鏡やCT下生検では生命に危険が及ぶような場合や、再発した部位が数㎜と採取するにはあまりに小さい微小再発例、採取が困難な脳などの部位へ再発したケースなどもある。
そのような場合は、血中の腫瘍細胞由来のDNAあるいはRNAを検出して行う、リキッド・バイオプシーがある。
血液の採取は、患部からの検体の採取に比べて安全であり、病理の全体像を把握しやすいと考えられており、リキッド・バイオプシーは新しい検査法の開発により検出感度が上がってきており、将来性を見込める方法の1つだという。ただし、血液と患部、どちらの検体が有効かについては、現状では結論に至る試験結果が出ていない。
進行したEGFR遺伝子変異陽性の非小細胞肺がんの再生検については、採取部位によってT790M変異の陽性率が異なるなど、抱える課題も多い。診断時生検に比べてほとんどの被検者の病状がより重篤であるだけに、手技の難易度が高く、その実施状況に関する情報も少ないのが現状のようだ。
効果が鈍ってきた時点で 早めに薬を切り替える
EGFR-TKIは比較的副作用が少ない薬であるため、効き方が鈍ってきた程度では使用が継続され、効果がなくなり明らかな悪化を認めてから、他の抗がん薬に切り替えることが多い。副作用の少なさを理由に、明らかに悪化を認めていても継続する医師もいる。しかし、木浦さんは、「以下は、私の経験に基づくお話であり検証されていませんが」と前置きした上で、次のように話す。
「私は少しでも効き方が鈍った時点で早めに再生検をし、T790M変異陽性であれば他のEGFR-TKIに切り替えるか、化学療法や他の治療を検討します」
今は、肺がんに使える薬が十数種類もある時代になった。それなのに、1970年代、薬の効果がなくなっても次に使う薬がなかった時代の薬剤切り替えのポイントが基本コンセプトにされている。
この奏効率の基準では、がんが10%大きくなってもSD(安定)の範囲にあり、20%以上大きくなってPD(進行)とみなし、ようやく薬を切り替えることになる。言い換えれば、はっきり悪化するまで薬効評価のために待つこととなる。
しかし、木浦さんは、例えば50だったがんの直径が、10まで縮小したとする。がんが耐性化し10あったがんが1増えたとしても(10%増大)、12までは待たず、11.1、11.2と、2度悪化したら薬を切り替える。
また薬物療法の経験が豊富な施設の場合に行える方法だが、例えば、耐性が生じた後に、抗がん薬を半年間ほど使用し、その後もう一度EGFR-TKIを使用することにより効果が期待できる場合もある。木浦さんのところでは、そのような方法で、1つのEGFR-TKIを総投与期間で2年間以上使うことができる患者さんも少なくないという。
耐性のタイプを見極めた治療選択を
第1世代、第2世代のEGFR-TKI耐性の治療戦略は、具体的には次のようになる。
まずは、安全が確保されれば可能な限り再生検をしてどの耐性のタイプかを見極める。耐性機序は大きく分けて、以下の❶~❹になる。
❶第1世代、第2世代のEGFR-TKIがEGFRに結合できなくなる
(1)T790M変異陽性あり⇒第3世代のEGFR-TKI
(2)T790M変異以外⇒通常化学療法
❷EGFR以外の側副シグナルが下流に入る
(1)理想的にはEGFR-TKIと側副シグナルを止めるEGFR-TKI
(2)通常化学療法
❸小細胞がん化
⇒通常化学療法
❹上皮間葉化
⇒通常化学療法
ただ、副作用については、AZD9291の使用中にも、間質性肺炎を発症する患者が5~6%いて、うち3分の1が死亡例となったと報告されているので、特に注意が必要だ。それ以外の副作用は比較的少ないと考えられている。
血管新生阻害薬アバスチンを加える可能性
耐性時の治療選択のもう1つの可能性は、血管新生阻害薬*アバスチンを用いる方法だ。前述のEGFR遺伝子変異のパターンのうち、エクソン19欠失変異と、エクソン19のL858R点突然変異のある場合に、イレッサやタルセバにアバスチンを併用すると、効果が高まるという。
イレッサとアバスチンの併用で完全奏効(CR)が得られた患者さんが5%ほどいたという結果が出ている。これらはすでに岡山大学で研究が進んでおり、論文として発表されている 1)。
さらに、今後様々な第3世代の薬が発売されると、第3世代薬を先にすべて使っていくのか、抗がん薬が先か、第1世代、第2世代、第3世代、抗がん薬の順で使用していくのか、多面的な角度からの研究と検証が必要になるという。
*アバスチン=一般名ベバシズマブ
1)Ichihara E, Hotta K, Kiura K. et al:J Thorac Oncol. 2015 Mar;10(3):486-91
治療薬がますます増える今後は 根治を目指す方向へ
「非小細胞肺がんの新しい治療法が増えつつある今、主治医とよく話をすること、セカンドオピニオンの検討も含めて、積極的に情報をキャッチしていただきたい」
このように願う木浦さんは、「主治医と共に闘うという姿勢は大切」と話す。
「医師としても、患者さんと一緒にやっているという実感があります。今は必ずどれか効く薬がありますので、いろいろ考えながら治療をしていきましょう。以前では考えられなかったくらいに治療法が進み、長期生存されている患者さん、10年を越えて闘病を続けておられる方もおられますから」
肺がん患者の年齢中央値は75歳を越えるが、同施設では若くして発症した人を数多く治療している。「そのような方々の治療は、延命ではなく治癒を目指す治療戦略を立てるべきと痛感しています」と話す木浦さん。
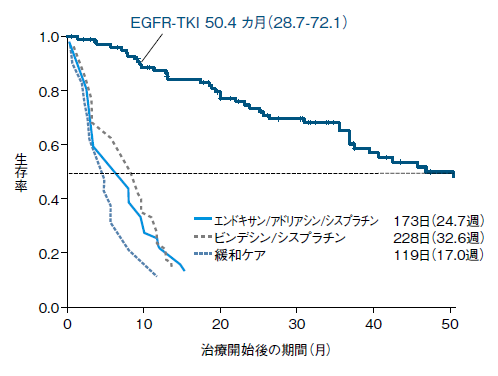
「進行肺がんで治癒を目指すと言えば、学会で随分叩かれた時代もありました。これだけ多くの新薬が出てきている今、少なくとも肺がんを専門とする施設ではEGFR遺伝子変異陽性の非小細胞肺がんの約半数は、5年を生きられることは当たり前でなければなりません」(図5)
木浦さんは、「これからは、『治りますよ』と患者さんに伝えてあげられる日がくることを目指しています」と今後の展望を語った。
(岡山大学病院、2002年10月~2011年10月)
同じカテゴリーの最新記事
- 手術後の再発予防に加え、Ⅲ期の放射線化学療法後にも EGFR変異陽性肺がんタグリッソの治療対象さらに広がる!
- 有効な分子標的薬がなかったEGFRエクソン20挿入変異陽性肺がんに ついに承認された二重特異性抗体薬ライブリバント
- 世界に先駆け初承認された分子標的薬ロズリートレクの課題 共通の遺伝子変異を標的とする臓器横断的がん治療薬
- 進行・再発卵巣がんに選択肢が増える 初回治療から分子標的薬リムパーザが使える!
- 肺がんに4つ目の免疫チェックポイント阻害薬「イミフィンジ」登場! これからの肺がん治療は免疫療法が主役になる
- 肺がん薬物療法最前線―― 分子標的薬と、オプジーボに代表される免疫チェックポイント阻害薬が、肺がん治療をここまで変えた!
- 第3世代タグリッソ登場で非小細胞肺がん治療はさらに進化
- 分子標的薬投入時期を「Window」で見える化 ホルモン陽性HER2陰性再発転移症例での適切な投与時期を示唆
- 非小細胞肺がん 耐性後は再生検を行い 適切なEGFR-TKIで治療する
- 深い寛解後に 70%が投薬中止可能~慢性骨髄性白血病の治療~


