世界に先駆け初承認された分子標的薬ロズリートレクの課題 共通の遺伝子変異を標的とする臓器横断的がん治療薬
高い奏功を示し 少人数の試験でも承認に
承認のもととなった主な臨床試験は、多施設共同非盲検国際共同第Ⅱ相バスケット試験の「STARTRK-2」(スタートレク・ツー)試験。同じ遺伝子変異を持つ患者さんを、がん種に関係なくひとつのかご(バスケット)に入れる臨床試験のことだ。ついでだが、1つの病に対し、複数の治療法を比較する試験は「アンブレラ試験」と呼ばれている。
ロズリートレクの場合、ROS1融合遺伝子、ALK融合遺伝子を有する症例にも効果が期待できるとして、試験の対象となったのはNTRK、ROS1またはALK融合遺伝子が陽性の局所進行または転移性固形がん患者さん。小児に多い肉腫なども対象とするため、18歳以上を対象としたSTARTRK-2試験と同時に、小児(22歳未満)対象の「STARTRK-NG試験」(海外Ⅰ/Ⅰb相試験)も行われた。
「STARTRK-2」の中間解析では、NTRKの有効性評価が可能な症例(51例)に対し、主要評価項目である奏効率は56.9%だった。
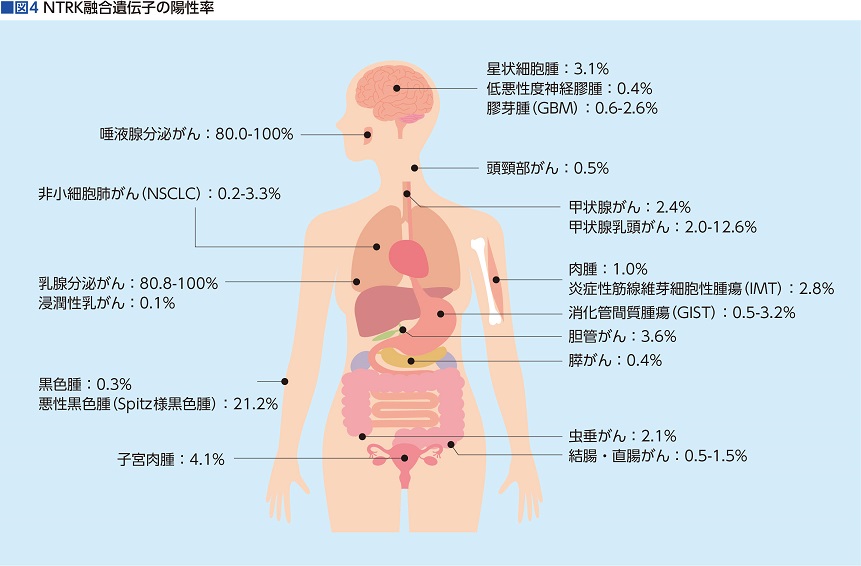
「肉腫、非小細胞肺がん、乳がん、唾液腺分泌がん、甲状腺がん、胆管細胞がんなど、様々な臓器のがん患者さんが集まりましたが、がんが半分以下になった(奏功割合)人が56.9%で、がんが消えてしまった人もいました。そこで、51例という少数にもかかわらず、NTRK融合遺伝子によってがんになった患者さんに承認されました」
有害事象は全体で205例(99.5%)に見られ、NTRK融合遺伝子陽性の固形がんの患者さんには100%(63例)見られた。主なものは便秘、味覚異常、疲労、浮動性めまいなど。重篤な有害事象は全体で81例(39.3%)見られ、2%以上に認められたものとして肺炎、胸水、呼吸困難など。NTRK融合遺伝子陽性の固形がんの患者さんでは30例(47.6%)に見られ、3例以上に認められたものとして低酸素症、肺炎、胸水など。
有害事象は強めと思われるが、「実際に使ってみて、特段強いということはなかったと感じています」と瀬戸さん。
小児対象のSTARTRK-NG試験では、NTRK融合遺伝子陽性の進行・再発小児固形がん患者5名にロズリートレクが投与され、類表皮性膠芽腫(こうがしゅ)ではがんが消える完全奏効(CR)、高グレード神経膠腫、悪性黒色腫、乳児型繊維肉腫でがんが30%以上小さくなる部分奏効(PR)、乳児型繊維肉腫で腫瘍サイズの変わらない(SD)という結果が得られた。
なお、STARTRK-2試験のうち、ROS1阻害薬による治療歴のないROS1融合遺伝子陽性の進行・再発非小細胞肺がん患者さんに対し、ロズリートレクの奏効率は75.8%に達した。そのため、2020年2月には上記非小細胞肺がんへの適応拡大になっている。
「ROS1融合遺伝子は肺がんにも多いが、最初に発見されたのは脳腫瘍(膠芽腫)で、胆管がんなど多くのがんに出現します。STARTRK-2試験でもロズリートレクに一定の奏功割合が認められましたが、肺がんに多いため、まず肺がんで適応がとれたということでしょう」
ロズリートレクのもうひとつの特徴は、脳転移のある人や脳腫瘍への有効性が高いことだ。STARTRK-2では脳転移のある人(10例)に対し、頭蓋内腫瘍奏効率が50%で、頭蓋内腫瘍の無増悪生存期間中央値(PFS)は14.3カ月という結果だった。また、小児でも脳腫瘍に奏効したことはすでに書いたとおり。
「脳転移のある人に効果的なのではありません。脳には血液脳関門があり、薬が移行しにくいという特徴がありますが、ロズリートレクは脳への移行性がいいので効くのです。例えば、進行・再発の非小細胞肺がんでは、ALKおよびROS1阻害薬のザーコリ(一般名クリゾチニブ)が先行していますが、ザーコリは脳に移行しないので脳転移への効果が劣ります」(図4)
標準治療後に遺伝子プロファイル検査が可能に
臓器横断的ながん治療が承認されたもう1つのメリットは、「標準治療が終わったあと、遺伝子プロファイル検査ができるようになったこと」という。
「目的は個別化医療の高度化、つまり、1人ひとりの患者さんに合った薬を届けることですが、現状は患者さんにどういう遺伝子変異が起きているかを見始めた段階。しかし、次世代シーケンサー(NGS:遺伝子の塩基配列を高速に読み取る解析機器)でがん種を超えて遺伝子変異が調べられるので、臓器横断的にどういう遺伝子変異が起きているか、わかってきていると思います。
例えば、肺がんでは2020年、METex14(METエクソン14スキッピング)変異のある非小細胞肺がんに対する初の治療薬として、テプミトコ(一般名テポチニブ)、タブレクタ(一般名カプマチニブ)が承認されましたが、こうした変異が肝臓でも起きていること、頻度は少ないが様々ながんに起きていることがわかれば、それに対する試験が行われ、薬が使われていく可能性があります。
同じように、BRAF遺伝子変異に対しては現在、皮膚がんと肺がんで保険適応になっていますが、これも臓器横断的な薬の開発に着手する製薬会社があってもいいかなと思います」
ハードルの高い「コンパニオン診断」がネックに
しかし、臓器横断的がん治療には、実際には非常に高いハードルがあるという。最大のハードルは患者数が少ないことだ。
「先にもふれましたが、肺がんの場合、EGFRやALKのようにメジャーな遺伝子変異があります。しかし、他のがん種ではそうした変異があまり見つかっていません。現在、標準治療が終わった後に遺伝子パネル検査をした人の10%くらいにしか治療薬はありません。非常に少数のがんのために、巨額な費用のかかる試験を行うことはむずかしいと言わざるを得ません」
もう1つ、大きなハードルとなっているのは、ロズリートレクを使うための「コンパニオン診断」(分子標的薬を使用するためにがん細胞異常を調べる検査)だ。ロズリートレクを使うには、米国で開発された「FoundationOne CDx がんゲノムプロファイル」による解析を受けることが必須となる。
これは、固形がん患者のがん組織又は細胞から得られたDNAデータを使い、324の遺伝子変異情報を解析するプログラム。ロズリートレクの販売元は2019年6月、そのコンパニオン診断としての承認を取得しているが、がん拠点病院とその関連病院でしか使えず、そのうえ、費用が高額(約50万円)と病院の負担などが大きく、一般病院では難しいとのこと。しかも、検体を米国に送らなければなない。
「もう少し安価な商品が承認されないと普及しないと思いますね。肺がん学会が出している『肺癌診療ガイドライン2019』にも、エヌトレクチニブ(ロズリートレク)について『FoundationOne CDx がんゲノムプロファイル』ができる施設が限られているので、使える患者さんが限定される〟と注意書きが記載されているくらいです」
「肺がんに関しては、すでに普及しているオンコマイン(コンパニオン診断の1つ)で遺伝子変異が確認された場合でも薬が使えるよう、企業も保険適応を取得しようとしています。また、先にお話ししたテプミトコ、タブレクタでは、オンコマインで遺伝子変異がわかった場合でも、FoundationOne CDxまたはArcherMETというコンパニオン診断を行わなければなりません。それでは困るというので、肺癌学会と肺がん連絡協議会が今、保険を見直してほしいと厚労省に申し入れているところです。新型コロナで遅れていますが、まもなく厚労省から回答があるはずです」
それでも検討したい遺伝子変異は続々 今後に期待したい
今日、NGSにより明らかになるがん関連遺伝子は増えるばかり。1人ひとりのがんの特徴が明らかになり、それに合った治療が組み立てられるオーダーメイド医療が主流になっていく。
「アメリカには〝マスターパネル・トライアル〟という治験システムがあり、遺伝子変異ごとに治験に振り分け、結果を見てよかったら承認する形になっています。日本でもロズリートレクのようなバスケット試験を、これまでわかっている主な遺伝子変異についてだけでも走らせられれば、ロズリートレクに続く臓器横断的な薬の適応がとれてくると思います」
今後薬剤開発の標的になっていくものとして、ALK、BRAF、BRCAness、FGFR、HER2、HER#、HRD、KRAS、RET、ROS1、TMB-highなどの融合遺伝子が挙げられているそうだ。数の少ない遺伝子変異を有するがんに対しても有効な試験システムを、ぜひ日本でも構築してほしい。
同じカテゴリーの最新記事
- 手術後の再発予防に加え、Ⅲ期の放射線化学療法後にも EGFR変異陽性肺がんタグリッソの治療対象さらに広がる!
- 有効な分子標的薬がなかったEGFRエクソン20挿入変異陽性肺がんに ついに承認された二重特異性抗体薬ライブリバント
- 世界に先駆け初承認された分子標的薬ロズリートレクの課題 共通の遺伝子変異を標的とする臓器横断的がん治療薬
- 進行・再発卵巣がんに選択肢が増える 初回治療から分子標的薬リムパーザが使える!
- 肺がんに4つ目の免疫チェックポイント阻害薬「イミフィンジ」登場! これからの肺がん治療は免疫療法が主役になる
- 肺がん薬物療法最前線―― 分子標的薬と、オプジーボに代表される免疫チェックポイント阻害薬が、肺がん治療をここまで変えた!
- 第3世代タグリッソ登場で非小細胞肺がん治療はさらに進化
- 分子標的薬投入時期を「Window」で見える化 ホルモン陽性HER2陰性再発転移症例での適切な投与時期を示唆
- 非小細胞肺がん 耐性後は再生検を行い 適切なEGFR-TKIで治療する
- 深い寛解後に 70%が投薬中止可能~慢性骨髄性白血病の治療~


