第2段階に入った分子標的薬の長所と短所 注意しよう! 従来の抗がん剤とは異なる優れた効果と思わぬ副作用
効くことが予測される患者さんに絞って投与
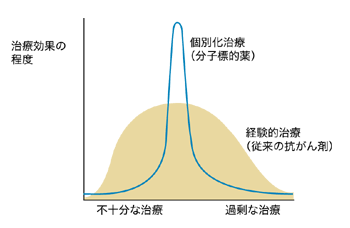
「もう1つは、標的分子が明確で限られていれば、あらかじめ投与前にその薬が効くかどうかを調べて、効果が予測できる患者さんだけに絞りこんで投与できる薬が現れたことです」(佐々木さん)
その代表はハーセプチンです。ハーセプチンは乳がん細胞に発現するHER2というタンパクを標的とした分子標的薬です。しかし、HER2が過剰発現しているのは乳がん全体の20~30パーセントにとどまるため、ハーセプチンはHER2過剰発現の乳がんには効きますが、過剰発現していない乳がんには効きません。あらかじめHER2過剰発現の有無を検査で確かめることで不要な投薬やそれによる副作用が避けられる一方、効くと推定される患者さんに絞って投薬できるようになったのです。
「ハーセプチンは乳がんの中でも悪性度が最も高い転移性乳がんに優れた効果を上げる分子標的薬として大きな注目を集めました。最近はHER2が過剰発現している早期乳がんの再発リスクを約50パーセント下げることも立証され、今まで最も予後が不良とされていたHER2過剰発現の乳がんが、最も治りやすい乳がんであるとさえ思わせるほど優れた効果をもたらしています」(佐々木さん)
| 従来の抗がん剤 | 分子標的薬 | |
|---|---|---|
| 作用機序 | DNAなどの合成や修復、細胞の分裂・増殖過程に作用し、がん細胞を殺す | がん細胞の増殖、転移などに関わる分子を標的にそれを阻害し、がんの増殖を抑えたり、進展を阻害する |
| がん細胞への特異的作用 | 低い | 高い |
| 抗腫瘍効果 | 期待 | 期待 |
| 種類 | アルキル化剤 抗生物質 代謝拮抗剤 植物アルカロイド | 血管新生阻害剤 シグナル伝達阻害剤 細胞周期調節剤 免疫療法、ワクチン |
| 長期投与 | できない | できる |
| 副作用(全般) | 重篤なものが多い | 特殊な副作用 |
| 骨髄抑制 | 高頻度 | ほとんど出ない |
| 心毒性、腎毒性、脱毛、口内炎 | 高頻度 | 薬により特徴的副作用 |
| 悪心・嘔吐 | 高頻度 | 消化器症状が出る場合も |
まったく歯が立たなかった悪性腫瘍にも優れた効果が
分子標的薬による進歩のあと1つは、従来の細胞毒性抗がん剤ではまったく歯が立たなかった悪性腫瘍に対して、優れた治療効果をもたらす薬が登場したことです。
「腎細胞がんに対するスーテントやネクサバールなどの分子標的薬がこれにあたります。両者はがん細胞の増殖を促す複数のタンパク(各種チロシンキナーゼ)を狙い撃つマルチキナーゼ阻害剤です」(佐々木さん)
腎細胞がんに効果的な抗がん剤はこれまで1つもありませんでした。代わってインターフェロンやインターロイキン2による免疫療法でしのいできたものの、その奏効率は15パーセント程度です。
「もちろん、延命効果が立証されたものは皆無で、手術で切除できなかったり再発したりした場合は有効な治療法がなかったのです。しかし、こうした腎細胞がんの治療をめぐる状況を一変させ、臨床試験で初めて延命効果を立証されたのがスーテントとネクサバールなのです」(佐々木さん)
事実、スーテントはインターフェロンやインターロイキン2などが効かなくなった患者でも34パーセントの奏効率を示し、無増悪生存期間が8.3カ月という優れた治療成績を上げています。また、ネクサバールはインターフェロンと比べた比較試験で、無増悪生存期間中央値を2カ月(ネクサバール7カ月、インターフェロン5カ月)延ばす治療成績を上げています。
分子標的薬による治療戦略は第2段階に
- 夢の薬ではない
- 増殖抑制だけではなく、腫瘍縮小効果をもたらすこともある
- 標的を多く持ったがんには効きやすいが、確実ではない
- 従来の抗がん剤とは異なった毒性
- 抗腫瘍効果をあらかじめ判定するマーカーはない
このように大きな成果を上げてきた分子標的薬ですが、その反面、新たな問題点も出てきました。分子標的薬に耐性が生じ、薬が効かなくなるという問題です。
「慢性骨髄性白血病に対するグリベックは、第1選択肢の治療薬としての位置を確立しています。症状の消失などの寛解状態を長期にわたって維持できるのですが、その一方、グリベックが効かなくなるという問題も新たに出てきました。しかし最近、この問題を解決する分子標的薬も新しく開発され、効果を上げだしています。それがスプリセルなどです」(佐々木さん)
欧米で行われた臨床試験では、スプリセルはグリベックの100~300倍ほど強力で、ほとんどの変異型のBcr-Abl遺伝子産生タンパクに効果があると期待されています。
タシグナはグリベックより10~30倍ほど強力で、スプリセルと比べて治療効果では若干劣るものの、副作用の少ないのが長所です。
グリベックは、慢性骨髄性白血病の原因であるBcr-Abl遺伝子産生タンパクを標的とする分子標的薬です。しかし、発病後さらにBcr-Abl遺伝子が突然変異を重ねると、変異型のBcr-Abl遺伝子産生タンパクがつくられるようになります。そのためグリベックは効かなくなってしまうのですが、この変異型Bcr-Abl遺伝子産生タンパクを狙い撃つようにつくりだされたのがスプリセルやタシグナで、これらは第2世代の分子標的薬になるようです。 「分子標的薬は狙い撃つ標的やその作用などが明確ですから、細胞毒性抗がん剤と比べて薬剤耐性のメカニズムも容易に調べることができます。そうした耐性のメカニズムを把握したうえでつくられたのが、第2世代の分子標的薬です」(佐々木さん)
初期に登場したハーセプチンやグリベックなどを第1世代とすれば、最近出始めているタイケルブやスプリセルなどの分子標的薬が第2世代だというのです。
第1世代の分子標的薬で表面化した問題点を新たに解決して出てきたのが第2世代です。さらに、薬の使い方でも新しい工夫が考え出され、分子標的薬同士を組み合わせて使う併用療法により治療成績を上げるという試みもスタートしています。そのことを考えると、分子標的薬による治療戦略は今や第2段階に入ったといえるでしょう。
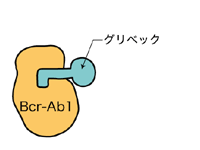
突然変異がないとグリベックは
Bcr-Ablのポケットに入り結合できる。
その結果、白血病細胞は死ぬ
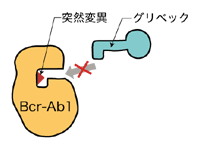
突然変異が起こるとグリベックは
Bcr-Ablのポケットに入れない。
その結果、白血病細胞が増える
同じカテゴリーの最新記事
- 手術後の再発予防に加え、Ⅲ期の放射線化学療法後にも EGFR変異陽性肺がんタグリッソの治療対象さらに広がる!
- 有効な分子標的薬がなかったEGFRエクソン20挿入変異陽性肺がんに ついに承認された二重特異性抗体薬ライブリバント
- 世界に先駆け初承認された分子標的薬ロズリートレクの課題 共通の遺伝子変異を標的とする臓器横断的がん治療薬
- 進行・再発卵巣がんに選択肢が増える 初回治療から分子標的薬リムパーザが使える!
- 肺がんに4つ目の免疫チェックポイント阻害薬「イミフィンジ」登場! これからの肺がん治療は免疫療法が主役になる
- 肺がん薬物療法最前線―― 分子標的薬と、オプジーボに代表される免疫チェックポイント阻害薬が、肺がん治療をここまで変えた!
- 第3世代タグリッソ登場で非小細胞肺がん治療はさらに進化
- 分子標的薬投入時期を「Window」で見える化 ホルモン陽性HER2陰性再発転移症例での適切な投与時期を示唆
- 非小細胞肺がん 耐性後は再生検を行い 適切なEGFR-TKIで治療する
- 深い寛解後に 70%が投薬中止可能~慢性骨髄性白血病の治療~


