適切な治療を、適切な患者に、適切な時に行うことが重要 個別化が進む世界のがん医療
個別化医療の質向上の鍵はマーカーの同定
確実に効果が得られる患者の判別が重要
乳がんは、個別化治療の進んでいるがんの1つである。ホルモン受容体、HER2受容体という治療標的が同定され、それぞれに対してホルモン療法、抗HER2療法という治療法が確立されている。最近ではさらに、ホルモン受容体陽性患者の中で、化学療法が有用である患者を判別するための多遺伝子解析検査も開発、応用されるようになっている。
こうした中にあって、現時点でもっとも予後不良とされるのがトリプルネガティブ乳がんだが、実は無治療の場合にもっとも予後不良なのはHER2陽性乳がんである(図4)。抗HER2薬ハーセプチンの登場によって、その予後が飛躍的に改善したのである。
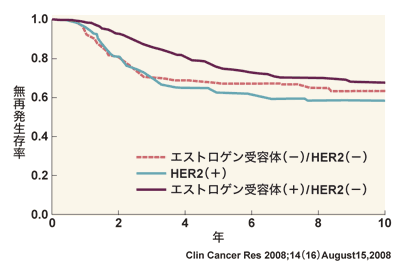
ただし、約20パーセントを占めるHER2陽性患者のうち、ハーセプチンが有効な患者は35~50パーセントで、乳がん全体では10パーセント程度に過ぎない。これについて、デューク大学のジョー・ネビンスさんは教育講演で、「ハーセプチンが有用な薬剤であることは言うまでもない。10パーセントの患者にしか効果がない薬剤だから失敗というわけではなく、生物学的観点にたてば、むしろそれが現実なのだ。がんの多くは非常に不均一な疾患だからである」と述べている。
個別化医療のためには、腫瘍の特徴から標的を定め、それに対する治療法を確立することに加えて、確実に効果の得られる患者を判別して投与することが重要だということだ。
たとえば、HER2陽性であっても、マーカーによってハーセプチンの効果が得られない患者を事前に判別できれば、乳がんの個別化医療はさらに進歩することになる。
大腸がんのKRAS遺伝子変異と同様のマーカーを求めて
上皮増殖因子受容体(EGFR)はさまざまながんに関わる因子であり、これを標的とするいくつかの分子標的薬が開発されている。EGFRを抑制するモノクローナル抗体のアービタックス(一般名セツキシマブ)、ベクチビックス(一般名パニツムマブ)や、EGFRのチロシンキナーゼを選択的に阻害するEGFR阻害剤イレッサ(一般名ゲフィチニブ)、タルセバ(一般名��ルロチニブ)などである。これらの薬剤について、現在効果予測マーカーの探索が精力的に行われている。
たとえば、大腸がんの治療に用いられるアービタックス、ベクチビックスは、KRAS遺伝子に変異がある患者には効果がないことが明らかになっている。そのため欧米ではすでに、これらの薬剤を用いる前に、患者のがん組織の遺伝子検査を行って、KRAS遺伝子変異があるかどうかを調べることが推奨されている。世界の経済状況を反映してか、今年の集会では医療コストについて言及する研究者が多かったが、シルスキーさんによれば、「KRAS遺伝子変異を有する大腸がん患者は40パーセントを占め、これらの患者に対する無用な治療を避けることで、米国では実に6億ドルの医療費削減につながる」という。患者にとっても社会にとっても個別化医療は望ましい、目指すべき医療の方向性といえそうだ。
EGFR変異の有無がイレッサの効果予測マーカーに
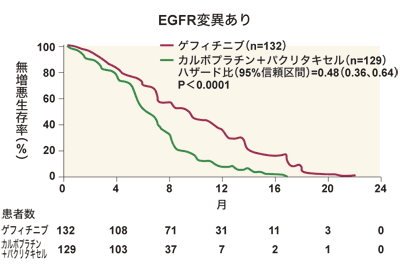
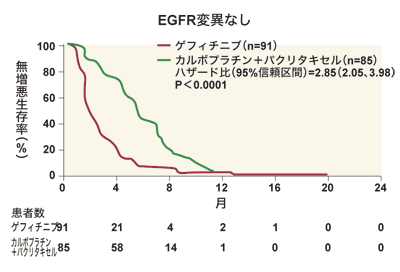
非小細胞肺がん治療においては、EGFR変異の有無がイレッサの効果予測マーカーになることが、近畿大学医学部堺病院腫瘍内科顧問の福岡正博さんから報告された。アジア人非小細胞肺がん患者を対象としたIPASS試験で、イレッサ治療群では、EGFR変異あり患者の無増悪生存期間は9.5カ月と、EGFR変異なし患者の6.3カ月と比較して良好であった(図5)。一方、標準療法群では、EGFR変異あり患者の無増悪生存期間は1.5カ月と、変異なし患者の5.5カ月と比較して不良であった。この成績から福岡さんは、「EGFR変異ありの患者では、副作用が少なく、経口投与可能なイレッサを第1選択にすべき」との見解を示した。
理論的で効果的な併用療法でがんの複雑性に対抗
今後の分子標的治療の方向性として重要なのは、新たな分子標的薬の開発だけでなく、どの薬剤がどのような患者で有効であるかを明らかにすることである。
ネビンスさんによれば、その理由は、効果を最大にし、不要な治療を避けることに加え、併用療法を理論的かつ効果的に行うためである。「単剤による治療は、これまでのところ大きな成功を収めていない。がんの複雑な生物学に対抗するためには、併用療法が不可欠である」という。またネビンスさんらは、経路活性化シグナチャー(個々の腫瘍でどの経路が活性化しているのかという特徴)をマーカーとする薬剤感受性の予測について研究を進めている。これまでに、同じシグナルが活性化されている腫瘍でも、下流のどのシグナル経路が重要な役割を果たしているかによって、薬剤感受性が異なることが明らかになってきているという。
経路シグナチャーによって、腫瘍をサブグループ化できるだけでなく、その腫瘍ではどの経路を阻害するのが効果的かという情報を手にできる。それは、新たな阻害薬開発や、個々の腫瘍で重要な役割を果たしている経路を標的とする分子標的薬の併用、いわば”経路標的治療”とでも言うべき戦略につながるものと言えるだろう。
同じカテゴリーの最新記事
- 有効な分子標的薬がなかったEGFRエクソン20挿入変異陽性肺がんに ついに承認された二重特異性抗体薬ライブリバント
- 手術後の再発予防に加え、Ⅲ期の放射線化学療法後にも EGFR変異陽性肺がんタグリッソの治療対象さらに広がる!
- PARP阻害薬や免疫チェックポイント阻害薬に続く トリプルネガティブ乳がんに待望の新薬登場!
- 免疫チェックポイント阻害薬の2剤併用療法が登場 肝細胞がんの最新動向と薬物療法最前線
- 新薬や免疫チェックポイント阻害薬も1次治療から 胃がんと診断されたらまずMSI検査を!
- リムパーザとザイティガの併用療法が承認 BRCA遺伝子変異陽性の転移性去勢抵抗性前立腺がん
- 免疫チェックポイント阻害薬で治療中、命に関わることもある副作用の心筋炎に注意を!
- SONIA試験の結果でもCDK4/6阻害薬はやはり1次治療から ホルモン陽性HER2陰性の進行・再発乳がん
- dose-denseTC療法も再脚光を ICI併用療法やADC新薬に期待の卵巣がん
- 心不全などの心血管の副作用に気をつけよう! 乳がんによく使われる抗がん薬


