希少肺がんのスクリーニングシステムを新薬開発につなげる
遺伝子診断ネットワークという革新的方法
このような状況の中、肺がんの個別化医療の推進に向け、後藤さんが中心となって日本で進めているプロジェクトがある。全国から肺がん患者さんのがん組織を集めて、EGFRやALKよりも希少なタイプのドライバー遺伝子を見つけ出して、新薬の臨床試験への参加に結びつけようという「遺伝子診断ネットワーク」だ。
「低い頻度で現れる遺伝子変化を拾い上げるためのシステムです。これまでにない革新的なシステムと言えます」
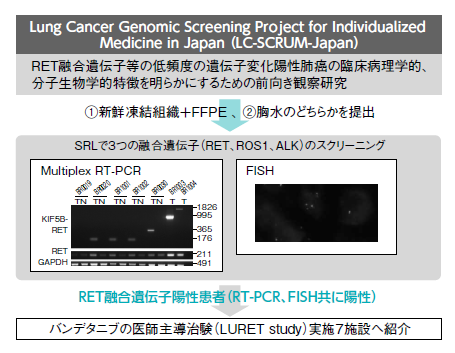
肺がんの希少なドライバー遺伝子を一元化して見つけようと13年2月に開始された。研究の正式名称は「RET融合遺伝子等の低頻度の遺伝子変化陽性肺癌の臨床病理学的、分子生物学的特徴を明らかにするための前向き観察研究」で、プロジェクト名は「LC(Lung Cancer;肺がん)スクラムジャパン」(図2)。ほかのがん種に先駆けた新しい取り組みとして注目されている。
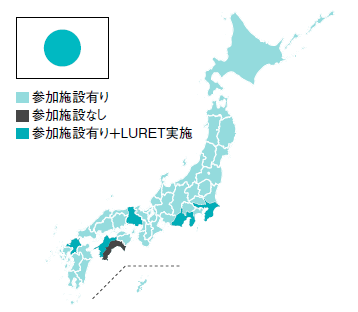
国立がん研究センター東病院を中心に、171の医療機関が参加(図3)。担当医がEGFR遺伝子変異のなかった(陰性)の患者さんに研究への参加を打診し、協力が得られた場合にがん組織の遺伝子解析を行う。2014年6月30日までに859例の登録があり(図4)、このうちRET肺がんが3%見つかっている。
このスクリーニングと併せ、医師主導治験として、RET融合遺伝子が陽性の肺がんを対象にしたvandetanibの第Ⅱ相臨床試験(LURET study)を全国7病院で実施している。条件を満たした患者さんはこちらに登録され、vandetanibの投与が受けられる。これまでに13人が登録されている。

産・官・学の連携で新薬開発に努力
「もし、ある希少なドライバー遺伝子を持つ肺がんの頻度がわずか1% であったとしても、日本では肺がんで年間約7万人が亡くなりますので、単純計算では700人もの患者さんが、この希少頻度の肺がんが原因で亡くなっていることになります。製薬企業は希少疾患に高額をかけて新��開発をすることは及び腰になりがちですので、医師主導の臨床試験が必要になります。それが私の所属する国立がん研究センターの役割です。希少肺がんにも有効な薬がありそうなので、それを開発して患者さんに届ける橋渡し役が『スクラム』の一番大きな役割です」
この試験ではRETのほかに、さらに頻度の低いROS1、BRAF遺伝子の変異も解析しているが、これら2つの遺伝子変異が見つかった場合は、企業主体の第Ⅱ相臨床試験への登録が可能となる。これらの治験では、ROS1融合遺伝子に対してはザーコリ、BRAF変異に対しては*dabrafenib(ダブラフェニブ、一般名)という有効性の高い薬剤を開発しているため、患者さんも有効な治療薬にたどりつける可能性が高くなります。
「典型的な産・官・学の連携です。このスクリーニングにより、企業による臨床試験も進み、患者さんに新薬を届けることができればと思っています。今は公的研究費に基づいてこのプロジェクトは進行していますが、今後は、多くの企業とのコラボレーション(共同研究)で遺伝子スクリーニングを継続していく予定です」
*dabrafenib(ダブラフェニブ)=商品名Tafinlar(タフィンラー)※米国では承認済み
複数のドライバー遺伝子を一度に解析する時代へ
さらに、これからは肺がんの複数のドライバー遺伝子を一挙に検査しようというマルチプレックス診断薬の登場が待ち望まれている。
「検査を1つひとつ行っていたら、何度も組織を採取する必要が生じ、また時間もかかってナンセンスです。一度の検査で複数のドライバー遺伝子がわかるような診断方法を研究中です。一度に短時間で多量の遺伝子を解析する技術革命です」
遺伝子解析には患者さんの協力も必要
肺がんの個別化医療の推進に向けて、医療側の体制作りは急ピッチで進んでいる。
後藤さんは、患者さんにも呼び掛けている。「遺伝子診断はとても大切です。病変部の組織を出来るだけ大きく取る必要があるために、気管支鏡や針を刺して組織を採取するような負担を伴う検査が必要になりますが、より良い治療を受けるために必ず通らなければならないことです。良い治療のためには患者さんも協力してもらわなければなりません。頑張っていただきたいと思います。
診断でターゲットがわかれば、漫然としたこれまでの抗がん薬治療ではなく、良く効いて副作用の少ない薬にたどりつくことが出来ます。患者さんのほうから、『私の肺がんには遺伝子変化はないですか』と医師に質問するくらいの関心を持っていただきたいと思っています」


