人工抗原のMUC1を使った免疫療法は、HLAに関係なく、誰でも受けられる 進行膵がんのMUC1療法
CTL&樹状細胞の併用で手術不能の膵がんに挑む
このように手術が可能な膵がん患者への有効性は認められたが、手術ができない患者や再発した患者への効果は不十分だった。
そのため山口大学ではCTL療法の効果を高めるため、樹状細胞(Dendoritic Cell=DC)を併用する免疫療法にも取り組んでいる。
樹状細胞は、T細胞などにがんの抗原を細胞の表面に押し出させる、専門的には抗原提示細胞と呼ばれる免疫細胞である。多くのリンパ球にがんの特徴を覚え込ませるという“教師”のような役割を果している。
リンパ球は直径10~15ミクロン(1ミクロンは1ミリの1000分の1)の小さな細胞で、血液1ミリリットルに約150万個入っている。その3分の2をT細胞が占めるのに対し、直径20~30ミクロンと比較的大きい樹状細胞は1パーセントと極端に少ない。免疫効果を出すには1回の投与で1億個の樹状細胞が必要と言われ、いかに増殖・活性化させるかが鍵になると言えるだろう。
先のCTL療法と同様、自分の腫瘍を用いる樹状細胞療法もあるが、山口大学ではMUC1を利用。人工的に作ったMUC1ペプチドを食べさせた後に樹状細胞を成熟化、つまりパワーアップさせる。
「そのパワーアップした樹状細胞により、効果的にMUC1-CTLを誘導するんです」(岡さん)
具体的には、患者の末梢血の中の単球から分離した未成熟な樹状細胞をインターロイキン4などを使って活性化。先のMUC1を取り込ませ、細胞の表面にMUC1を押し出した樹状細胞(MUC1-DC)を10日で完成させる。
静脈注射するCTLと異なり、それを患者の大腿部の付根に接種する理由は、樹状細胞がT細胞の多いリンパ節に移動してT細胞にがんの特徴を教え込む特徴があるためだ。体内に注入後にもT細胞などのリンパ球を活性化する免疫反応が起きるという仕組みだ。
大きな腫瘍や局所再発には効力に限界
CTL&DC療法の治療前後]
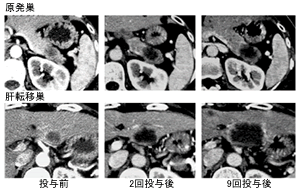
のCT画像に変化がなく、安定した状態だった
[肝転移した木元さんの腫瘍マーカーの推移]
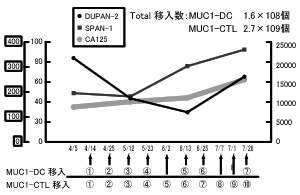
木元春江さん(仮名)が、山口大学附属病院を訪れたときにはすでに膵がんが肝臓に転移し、切除が不可能な状態だった。木元さんは、高度先進医療のMUC1で誘導するCTL&DC療法に臨んだ。
通常、肝転移や腹膜播腫(腹膜にがん細胞が散らばること)など切除ができない膵がん患者の1年生存率は10パーセントに満たない。しかし、木元さんは、6カ月もの間、膵臓と肝臓のCT画像には全く変化が見られない。計15回の投与で安定した状態を過ごした後、容体が悪化して1年後に亡くなった。
「この療法は大きな可能性を秘めていますが、過度の期待をかけられても困ります。何より副作用や治療による苦しみがなく、QOLが良好に保たれるのが大きな魅力なんです」(岡さん)
現在までに切除不能・再発膵がん12人にMUC1で誘導するCTL&DC療法を実施、繰り返し投与したところ、術後に肺転移を起こした方1人に著効、肝臓に転移した木元さんに6カ月の無変化を認めている。
MUC1で誘導するCTL&DC療法が、切除不能な膵がんにも少し効果があることは示しているものの、大きな腫瘍や局所再発には効力の限界があることも明らかになった。
「局所の制御に関しては、樹状細胞の局所投与やワクチン療法など、他の免疫療法の併用など、さらに工夫が必要です。また、進行膵がんの第1選択薬になっている抗がん剤のジェムザールなどとの併用も行って行きたいと考えています」(岡さん)
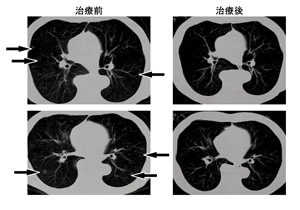
6回の治療後(右)治療後、肺転移は完全に消失した
これらの高度先進医療は、1回の投与につき12万6700円の費用が患者の自己負担になる。高度先進医療は例外的に混合診療が認められており、免疫療法の全額負担+通常の健康保険適応のがん治療費という形での支払いになる。
高度先進医療の治療費については、一定額を超えれば超過分が払い戻される高額療養費制度は適用されないなど、患者にとって負担が大きいと言わざるを得ない。
副作用がほとんどなく、患者のQOLを保ってくれる魅力的な治療なだけに、さらなる発展を期待したい。
同じカテゴリーの最新記事
- 1人ひとりの遺伝子と免疫環境で治癒を目指す! がん免疫治療が進んでいる
- 自分の免疫細胞も活用してがんを攻撃 PRIME CAR-T細胞療法は固形がんに効く!
- 頭頸部がんに対する「光免疫療法」の第Ⅲ相試験開始 第Ⅱ相試験の好結果を受け、早期承認への期待高まる!
- 白血病に対する新しい薬物・免疫細胞療法 がん治療の画期的な治療法として注目を集めるCAR-T細胞療法
- 進行膵がんに対する TS-1+WT1ペプチドパルス樹状細胞ワクチン併用療法の医師主導治験開始
- がん患者を対象とした臨床試験で証明された、米ぬか多糖体(RBS)の免疫賦活作用
- 先進医療の結果次第で、大きく進展する可能性も! 進行・再発非小細胞肺がんに対するNKT細胞療法
- 現在3つのがん種で臨床試験を実施中 がんペプチドワクチン療法最前線
- 免疫力アップで照射部位から離れた病巣でもがんが縮小 アブスコパル効果が期待される免疫放射線療法


