抗がん剤の効果と副作用を予測するだけでなく、予後も予測する 個別化医療の実現を可能にするバイオマーカーに大きな期待
イレッサでバイオマーカーの有効性を改めて認識
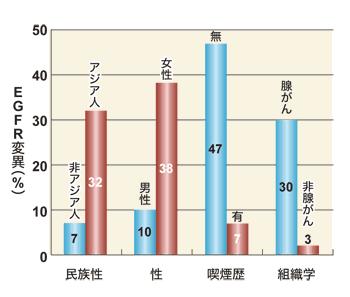
一方、バイオマーカーと分子標的治療薬の関係を改めて認識させたのが、肺がん治療薬のイレッサ(一般名ゲフィチニブ)だ。イレッサは、当初「東洋人、女性、喫煙歴がない、腺がん」という条件に当てはまる人に効果が高いことが示された。いったい、この条件にはどういう意味があるのだろうか。それが、EGFRの遺伝子変異にあるとわかったのは2004年のことだ。EGFRは細胞膜を貫通するタンパクで、細胞表面のEGFRにリガンドが結合すると、細胞増殖シグナルがオンになる。イレッサは、このシグナルをブロックする分子標的治療薬として開発された。しかし、実際にはEGFRの遺伝子変異がある人に効いていたのである。
具体的には、エクソンの19番の遺伝子に欠損があると80パーセントぐらいに効果がある。21番に突然変異があると71パーセントの人に効果がある。逆に変異がない人には1パーセントぐらいしか効果がない。前述のイレッサがよく効く人には、こうした遺伝子変異が多いという共通項があったのだ。逆に、790番目の塩基に変異があると、前記の変異があっても効果がないこともわかった。イレッサの投与を続けていると、効かなくなることがあるが、こういう人には後天的に790番目の変異が起きていることが多いのだ。
最近、非喫煙者で進行した腺がんのアジア人の非小細胞肺がんの初回治療の患者を対象に、標準治療であるタキソール(一般名パクリタキセル)とパラプラチン(一般名カルボプラチン)の併用療法とイレッサ単独での無増悪生存期間を比較する試験(IPASS試験)が行われた。その結果、イレッサを投与した群の中でEGFRの変異がある人は無増悪生存期間が9.5カ月と1番長く、逆に変異がない人は1.5カ月で抗がん剤併用群の5.5カ月より生存期間が短いことがわかった。つまり、EGFRの変異がイレッサの効果を予測する重要なバイオマーカーであることが、確認されたのである。
なお、イレッサやハーセプチンの適応の有無をみる遺伝子診断は、すでに保険で認可されている。内視鏡などで腫瘍組織を採���して、検査が行われる。
注目されるKRASの遺伝子変異
一方、新たなバイオマーカーとして注目されているのが、細胞分裂に係わるKRAS(ケイラス)遺伝子だ。
大腸がんの分子標的治療薬アービタックス(一般名セツキシマブ)もEGFRに結合してがんの増殖を防ぐ抗体薬で、単剤もしくは従来の抗がん剤と併用すると無増悪生存期間が有意に延びることが、多くの臨床試験で明らかとなっている。ところが、KRAS遺伝子に変異があるとアービタックスが効かないことがわかってきた。イレッサも、KRASに変異があると効果がないことが示唆されている。
「野生型のKRASを有する場合は、緩和治療を行うよりアービタックスを投与したほうが延命効果が上乗せされるのですが、KRASの変異があると上乗せ効果がないのです」と藤田さんは語る。
そこで、アメリカでは、KRASの変異を調べた上でアービタックスを投与している。実際には、切除不能の大腸がん患者の4割近くに、KRASの変異があるそうだ。ところが、日本ではまだKRASの遺伝子診断が保険で認められていないため、高価な薬を効かない人にも無選別に投与している医療機関が多いのが現状だ。
この他、慢性骨髄性白血病の治療を大きく変えたグリベック(一般名イマチニブ)は、長期間毎日服用することになる。このとき、服用前の1番薬の血中濃度が低下した状態(トラフ値)が高い人のほうが、効果が高い可能性があり、グリベックのバイオマーカーとして期待されているそうだ。
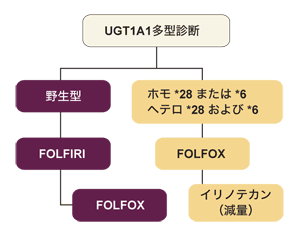
そして、冒頭にもあげた殺細胞性抗がん剤、塩酸イリノテカンは大腸がんや直腸がんの転移や再発に広く使われているが、白血球や好中球の減少と遅延性の激しい下痢が、患者を苦しめる。本来、塩酸イリノテカンはUGT1A1という酵素の働きで肝臓でグルクロン酸抱合(薬物投与における解毒作用の1つ)を受け、無毒化されて胆汁から腸に排出される。
ところが、この酵素の遺伝子に変異(28番と6番)があると、酵素の発現や活性が低下してグルクロン酸抱合能力が低下し、重い副作用が出る可能性が高くなる。「これらの変異がある人は毒性が約5倍も高くなるのです」と藤田さん。
そこで、日本でも遺伝子診断で該当する変異があれば、投与量を下げるように勧告されている。逆にいえば、グルクロン酸抱合が効率よく行われないので、こういう人は少量でも薬が効きやすいかもしれないのだ。
なお、この遺伝子診断は血液検査で行われ、日本でも保険で認可されている。埼玉医大では、保険認可に先立って2005年より、400人以上の患者さんに遺伝子診断を行い、治療方針の決定に役立てている。
薬の開発、臨床試験の効率化へも大きな期待

(写真は商品名Applied Biosystems SOLiD 3Plus システム)
この他、殺細胞性抗がん剤では白血病治療薬ロイケリン(一般名メルカプトプリン、薬剤略語6MP)でも代謝酵素(TPMP)の遺伝子多型で解毒の効率に差があること、したがって多型の頻度の高い欧米人においては遺伝子診断による投与量の調整が必要とされている。乳がん治療に使われるノルバデックス(一般名タモキシフェン)でも、CYP2D6という薬物代謝酵素の欠損で効果が低下し、再発が増えるのではないかと言われているが、これがバイオマーカーになるかどうかはまだ検討中の段階だ。
さらに、細胞増殖などシグナル伝達の中間に位置するMTORなども今後のバイオマーカーとしての利用が研究されているそうだ。
藤田さんは「バイオマーカーを使って効果と副作用の予測のもとに、治療方針を決め、抗がん剤を選択する。それによって、がん治療の大きな目標である個別化医療を実現できる可能性はあると思います。それだけではなく、バイオマーカーは薬の開発や臨床試験を効率化するという点でも大きな期待を集めています」と語る。
抗がん剤などの開発は、完成間近の段階で失敗するほどコストがかかり、それが開発のネックになっている。バイオマーカーを利用して薬の作用と副作用を予測し、臨床試験を行えば、より薬の開発がスピードアップする。その点でも、バイオマーカーへの期待は大きい。

同じカテゴリーの最新記事
- 正確な診断には遺伝子パネル検査が必須! 遺伝子情報による分類・診断で大きく変わった脳腫瘍
- 高濃度乳房の多い日本人女性には マンモグラフィとエコーの「公正」な乳がん検診を!
- がんゲノム医療をじょうずに受けるために 知っておきたいがん遺伝子パネル検査のこと
- AI支援のコルポスコピ―検査が登場! 子宮頸がん2次検診の精度向上を目指す
- 「尾道方式」でアプローチ! 病診連携と超音波内視鏡を駆使して膵がん早期発見をめざす横浜
- 重要な認定遺伝カウンセラーの役割 がんゲノム医療がますます重要に
- 大腸のAI内視鏡画像診断が進化中! 大腸がん診断がより確実に
- 「遺伝子パネル検査」をいつ行うかも重要 NTRK融合遺伝子陽性の固形がんに2剤目ヴァイトラックビ
- 血液検査で「前がん状態」のチェックが可能に<img draggable="false" class="emoji" alt="⁉" src="https://s.w.org/images/core/emoji/11/svg/2049.svg"> ――KK-LC-1ワクチン開発も視野に


