アロマターゼ阻害剤で有効性を示す新たな結果も
再発を防ぐために――乳がん術後治療の最新トピック

藤田保健衛生大学
医学部乳腺外科教授の
内海俊明さん
目に見えないがんを叩くため、乳がんの治療は手術だけではなく、術後治療による全身療法が非常に重要となってくる。
術後治療の基本的な考え方をおさえるとともに、最新のホルモン療法についても紹介する。
目に見えないがんを叩くために術後治療が重要
乳がんの治療は、手術だけで終了になることはあまりない。多くの場合、術後治療として、ホルモン療法や化学療法が行われている。こうした治療が必要になるのは、手術が行われる時点で、がん細胞がすでに他の臓器に転移している可能性があるからだ。
藤田保健衛生大学医学部乳腺外科教授の内海俊明さんは、次のように説明してくれた。
「日本人の乳がんの多くは乳管に発生します。がんが管の内側におさまっていれば非浸潤がん、管を取り巻く基底膜を破って外に出ていれば浸潤がんといいます。浸潤がんになると、血管やリンパ管にがん細胞が入り込み、遠隔臓器やリンパ節に転移するようになります。そこで、たとえ画像検査などで転移巣が見つかっていなくても、浸潤がんの場合には、再発を予防するために術後治療が行われるのです」
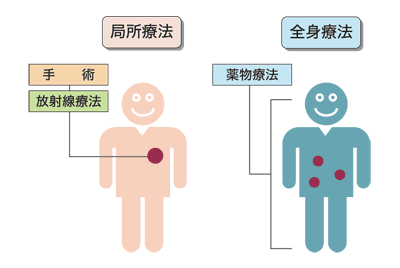
乳がんの治療には、局所療法と全身療法に分けられる(図1)。どこにあるか見えない転移巣を攻撃するためには、全身療法が必要になる。手術に加え、化学療法やホルモン療法などが行われるのは、こうした理由からだ。
ターゲットをより明確にして治療法を選択
乳がんの治療に関しては、「ザンクトガレン国際専門家合意会議」における合意事項が、重要な指針となっている。会議は2年に1度開かれ、そこで国際的に評価された最新の治療法が発表されている。
術後治療に関しては、07年の会議で大きく変わった。それまでは、まず再発リスクに注目し、リスクが高い患者さんには抗がん剤を含めた治療を行うことになっていた。ところが、07年からは、まず治療ターゲットを定め、さらに再発リスクも検討して、治療が行われるようになったのだ。
「09年の会議では、治療ターゲットに閾値(*)を設け、それに基づいて治療法を選択するようになりました(図2)。そこが、07年までと変わったところです」
*閾値=限界値のこと
| 治療手段 | 適応 |
|---|---|
| ホルモン療法 | エストロゲン受容体染色が少しでも陽性なら |
| 抗HER2療法 | 米国臨床腫瘍学会/米国病理医会ガイドラインに準ずるHER2陽性 |
| 化学療法 | |
| HER2 陽性疾患 (抗HER2療法を併用) | 臨床試験のエビデンスはトラスツズマブ使用は化学療法と同時または順次併用に限定 |
| トリプルネガティブ | ほとんどの患者 |
| エストロゲン受容体陽性、 HER2陰性+ホルモン療法 | リスクに応じて様々(図3参照) |
治療ターゲットを有する治療には、ホルモン療法と抗HER2療法がある。抗HER2療法とは、分子標的薬ハーセプチン(一般名トラスツズマブ)による治療のことだ。
「たとえばホルモン療法であれば、エストロゲン受容体が少しでも陽性ならホルモン療法を行いましょう、という内容になっています。少しでも陽性なら、という閾値を設けたところが、09年の合意の特徴です」
ホルモン療法と異なり、化学療法にはターゲットがない。そこで問題となるのが、エストロゲン受容体が陽性で、HER2が陰性の場合だ。ホルモン療法だけでいいのか、あるいは化学療法も行ったほうがいいのか、判断が難しくなる。
結論から言えば、エストロゲン受容体の発現レベル、組織学的グレード、増殖のレベル、腋窩リンパ節転移などの要素を考慮した上で、治療法を選択することになっている(図3)。
| 化学・ホルモン療法の 相対的適応 | 決定には役立たない 因子 | ホルモン療法単独の 相対的適応 | |
|---|---|---|---|
| エストロゲン受容体および プロゲステロン受容体の発現状況 | 低い | 高い | |
| 組織学的グレード | グレード3 | グレード2 | グレード1 |
| 増殖 | 高い | 中間 | 低い |
| 腋窩リンパ節転移 | 4個以上 | 1-3個 | 陰性 |
| 腫瘍周囲の脈管浸潤(PVI) | 広汎なPVIがある | 広汎なPVIがない | |
| 病理学的腫瘍径 | >5cm | 2.1-5cm | ≦2cm |
| 患者の選好 | 使用可能なすべての 治療を希望 | 副作用は避けたい | |
| 多遺伝子発現分析 | |||
| 遺伝子シグニチャ | 高得点 | 低得点 | |
新しい解析方法で有効性が証明された
乳がんのホルモン療法は、エストロゲンとエストロゲン受容体とを、鍵と鍵穴に例えると理解しやすい。エストロゲン受容体はがんの増殖という扉を閉める鍵穴。ここにエストロゲンという鍵が差し込まれると、扉が開いてがんの増殖が始まるのだ。
ホルモン療法には2つの方法がある。1つは、鍵穴を塞ぎ、鍵が入らなくする方法。もう1つは、鍵穴はそのままにして、鍵をなくしてしまう方法だ。
鍵穴をふさぐ働きをする薬を抗エストロゲン剤といい、タモキシフェン(一般名ノルバデックス等)がよく知られている。
一方、鍵をなくしてしまう方法、つまりエストロゲンをなくす薬は2種類ある。閉経前の人が使うのが、LH-RHアゴニスト。卵巣の機能を止める働きを持っている。これに対し、閉経後の人に使うのがアロマターゼ阻害剤である。
閉経後、卵巣は機能しなくなるが、副腎で作られるアンドロゲンが、アロマターゼという酵素の働きでエストロゲンに作り替えられる。アロマターゼ阻害剤は、この酵素の働きを抑えることで、エストロゲンができないようにするのである。
現在使われているアロマターゼ阻害剤には、フェマーラ(一般名レトロゾール)、アリミデックス(一般名アナストロゾール)、アロマシン(一般名エキセメスタン)の3種類がある。
BIG1-98という臨床試験では、フェマーラとタモキシフェンの比較が行われてきた。たとえば、閉経後の患者さんが、術後治療としてタモキシフェン5年服用と、フェマーラ5年服用では、どちらが再発予防に効果的かを調べる比較試験が行われている。もともとタモキシフェン5年間が標準治療とされていたが、閉経後の患者さんには、フェマーラのほうが効果的であることがわかった。
「フェマーラのほうが明らかにいいことが分かったので、そのまま試験を続行するのは倫理的に問題だということでタモキシフェン服用群は盲検解除になり(タモキシフェンを飲んでいるかを明らかにすること)、タモキシフェン服用の人でも、希望があればフェマーラに変えられることになりました。そのため、タモキシフェンを飲んでいた人の約25パーセントが、フェマーラに乗り換え、単純な比較ができなくなってしまったのです」
乗り換えたことを考慮せずに両群をそのまま比較する解析方法や、乗り換えた人を除外して比較する解析方法があるが、どちらも正確な結論には至らない。そこで、タモキシフェンを継続した患者情報に比重を置き、いろいろなバイアスを調整するIPCWという方法で解析が行われた。その結果、フェマーラのほうが再発予防だけでなく、生存率も優れている可能性が示されたのだ(図4)。

試験開始時点で予定していなかった解析を行っているわけで、この方法は統計的に問題がないわけではない。
しかし、盲検解除になった臨床試験では、こうした解析を行うことも必要だと考えられているようだ。
同じカテゴリーの最新記事
- 高濃度乳房の多い日本人女性には マンモグラフィとエコーの「公正」な乳がん検診を!
- がん情報を理解できるパートナーを見つけて最良の治療選択を! がん・薬剤情報を得るためのリテラシー
- 〝切らない乳がん治療〟がついに現実! 早期乳がんのラジオ波焼灼療法が来春、保険適用へ
- 新規薬剤の登場でこれまでのサブタイプ別治療が劇的変化! 乳がん薬物療法の最新基礎知識
- 心臓を避ける照射DIBH、体表を光でスキャンし正確に照射SGRT 乳がんの放射線治療の最新技術!
- 術前、術後治療も転移・再発治療も新薬の登場で激変中! 新薬が起こす乳がん治療のパラダイムシフト
- 主な改訂ポイントを押さえておこう! 「乳癌診療ガイドライン」4年ぶりの改訂
- ステージⅣ乳がん原発巣を手術したほうがいい人としないほうがいい人 日本の臨床試験「JCOG1017試験」に世界が注目!
- 乳がん手術の最新情報 乳房温存手術、乳房再建手術から予防的切除手術まで
- もっとガイドラインを上手に使いこなそう! 『患者さんのための乳がん診療ガイドライン』はより患者目線に



