分子標的薬ペマジール承認から1年、遺伝子検査のタイミングも重要! 切除不能の胆道がん薬物療法最前線

長きに渡って、ゲムシタビン、シスプラチン、S-1という3剤の抗がん薬しか治療法がなかった胆道がん薬物療法に、明るい兆しが見えてきた。2021年3月に承認された初の分子標的治療薬ペマジールが臨床に登場しておよそ1年。加えて、まだ臨床試験段階ではあるが、免疫チェックポイント阻害薬を含む併用療法の開発も進みつつある。
膵がんと並んで難治とされる胆道がんだが、今後、どのような展開が期待できるだろうか。胆道がん薬物療法の最新知見と今後の展望について、神奈川県立がんセンター消化器内科部長の上野誠さんに話を聞いた。
胆道がんは発生箇所によって性質が違う
胆道は、消化酵素の1つである胆汁が運ばれる道。胆汁は、肝臓内で、無数の肝細胞から生成されるので、胆道のスタート地点は肝臓の中となる。
肝臓内に細かく張り巡らされた細い管として始まった胆管は、肝臓内で作られた胆汁を運びながら合流を繰り返し、徐々に太くなっていく。そして、肝臓から外に出た地点(肝門部)で1本の管にまとまり、胆汁を十二指腸へ運んでいく。途中、胆汁を濃縮し、溜めておく貯蔵庫が胆のうだ。
肝臓内の胆管を肝内胆管、肝臓から外に出ている胆管を肝外胆管と称し、肝外胆管は十二指腸との繋ぎ目である十二指腸乳頭部まで続く。十二指腸乳頭部の直前では膵臓の中を通り、膵液を運ぶ膵管とともに、十二指腸へ繋がる仕組みになっている。
これが胆汁の誕生から十二指腸へ受け渡されるまでの道筋。この道を総称して「胆道」と呼ぶわけだが、胆道がんは、がんができた場所によって名称が変わり、その性質にも違いが生じるという特徴を持つ。
肝臓内の胆管に発症したがんは「肝内胆管がん」。肝門部の近辺に発症すると「肝門部領域胆管がん」、そして、肝臓から外に出て十二指腸へ向かう途中に発症すると「肝外胆管がん(遠位側胆管がん)」、胆汁の貯蔵庫である胆のうに発症すると「胆のうがん」、十二指腸と胆管の境目である十二指腸乳頭部に発症すると「十二指腸乳頭部がん」となる(図1)。
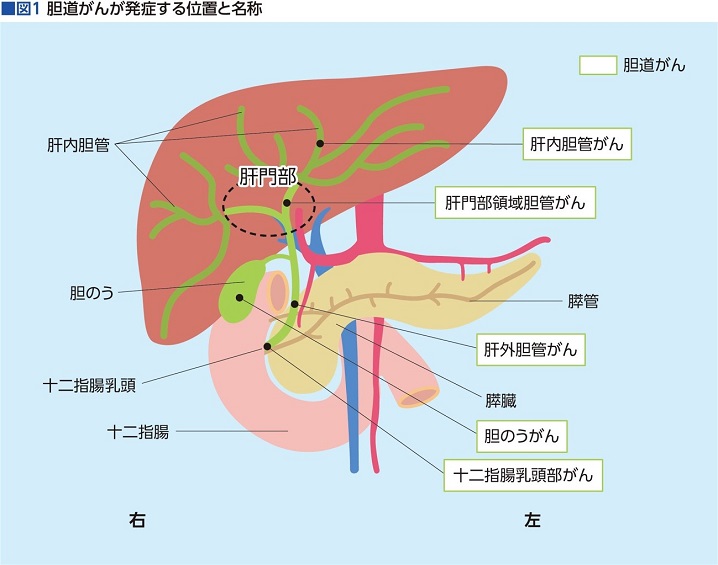
発症箇所によって名称が異なり、それぞれに特有の性質を持つ胆道がんの薬物療法は、一筋縄ではいかない。それを表すかのように、多くのがん種が薬物療法において進化の一途をたどる中、切除不能の胆道がんについては、長く進展のない状態が続いていた。
ところが、ここ数年、そんな状況に変化の兆しが見えてきたのだ。
切除不能胆道がんの標準治療とは
その前に、標準治療について確認しておこう。
切除不能の胆道がんに対する標準治療は、細胞障害性抗がん薬の併用療法。ゲムシタビン(商品名ジェムザール)、シスプラチン(同プリプラチン/ランダ)、S-1(同TS-1)を、2剤、もしくは3剤併用する。ゲムシタビン+シスプラチン(GC療法)、ゲムシタビン+S-1(GS療法)、もしくはゲムシタビン+シスプラチン+S-1(GCS療法)を、効果を見ながら繋いでいくという手法をとる。
「切除不能の胆道がんに対する薬物療法といえば、この3剤のみという状況が、かなり長い期間、続いてきました。もちろん、臨床試験は多々行われてきたのですが、3剤の組み合わせ以外、10年以上は進展が見られなかったというのが実情です」と神奈川県立がんセンター消化器内科部長の上野誠さんは語る。
ゲノム医療の進化から分子標的治療薬の開発へ
そんな状況に一石投じたのは、ゲノム医療の進歩だったと上野さんは指摘する。
「胆道がんに対する分子標的治療薬は10年ほど前から海外で注目されて、臨床試験も行われてきましたが、うまくいかず中断したままでした。そんな中、世界的にゲノム医療が進歩し、特定の遺伝子発現がある人を見つけ出し、その遺伝子発現にピンポイントに作用する分子標的治療薬を使うことが可能になってきたのです。この動きこそが、胆道がんにおいても分子標的治療薬の開発をいっきに押し進めたと言えるでしょう」
最初は、肺がんなどから分子標的治療薬の開発が進み、さまざまながん種へと拡大されていった。胆道がんにも、その流れがようやく巡ってきたのだ。
FGFR阻害薬ペマジールのメカニズム
胆道がんに現在使える分子標的治療薬としてもっとも注目すべきは、FGFR阻害薬のペマジール(一般名ペミガチニブ)。FGFR2融合遺伝子変異を持つ切除不能の胆道がんの2次治療として、2021年3月に承認された。
「FGFR2融合遺伝子に変異があるということは、がんが増殖する回路に常にスイッチが入ってしまっている状態。つまり、がんが増殖し続けてしまうのです。そのスイッチを切るのが、FGFR阻害薬です」と上野さんは説明し、さらに続けた。
「がんが増殖する回路のスイッチは、いろいろあります。ただ、影響の大きい主電源のようなスイッチを持つ人の場合、それさえ切れば、がんの増殖を止めることができます。そうした主電源に当たるものを『ドライバー遺伝子』と呼びます。たくさんのスイッチをバラバラと持つ人は、1つのスイッチを切ってもあまり効果は期待できませんが、主電源(ドライバー遺伝子)を持つ人を見つけ出し、そのスイッチを切る。これがゲノム医療に基づいた分子標的治療薬なのです」
「融合遺伝子」と名のつくものの多くがドライバー遺伝子。つまり、FGFR2融合遺伝子に変異がある人は、がんを増殖させる回路の主電源が常にオンになっている状態で、FGFR阻害薬ペマジールは、その主電源を切る役目を果たす薬剤というわけだ。
ペマジールの恩恵を受けられる頻度と意味
ペマジールが適応となるFGFR2融合遺伝子変異が見られるのは、主に肝内胆管がん。まれに肝門部領域胆管がんでも見られることはあるが、残念ながら肝外胆管がんにはまず見られない。
ただ、肝内胆管がんに見られると言っても、その頻度は7~13%ほどと言われている。「実臨床の印象では、肝内胆管がん全体の5%ほどの印象です」と上野さん。そもそも、肝内胆管がんは、胆道がん全体のおよそ5~10%程度と頻度が低い。つまり、現状においては、FGFR2融合遺伝子変異が見つかって、ペマジールの恩恵を受けることができる人は決して多くはない。
とはいえ、ペマジールは胆道がんにおける分子標的治療薬の最初の1歩。現時点ではFGFR2融合遺伝子変異以外だと、MSI-Highなど限られているが、今後、ゲノム医療がさらに進み、ドライバー遺伝子の数が増えれば、それに対する分子標的治療薬の開発も進むだろう。そうなれば、1つひとつの分子標的治療薬に該当する確率は低くとも、それらのうちどれかに該当する確率は増えていく。
「まさにそれを体現しているのが、肺がんです」と上野さん。分子標的治療薬の開発が先行している肺がんでは、複数のドライバー遺伝子が解明され、それらにピンポイントに作用する分子標的治療薬が次々に開発されていることで、長く生存できる人が増えている。
「ペマジール1剤だけの現状では高頻度の的中は期待できませんが、今後、肺がんのように治療を広げていけるようになるために、まず重要な1歩を踏み出したことは確かだと思います」
今後、FGFR2融合遺伝子に続くドライバー遺伝子として、IDH、BRAF、HER2などの解明が期待されている。
同じカテゴリーの最新記事
- 本邦初「肝内胆管癌診療ガイドライン2021」誕生! 肝内胆管がんの薬物療法はこれまでにないスピードで進化中
- 年1度の超音波検査が早期発見のカギ 胆のうがんは早期に見つければ95%完治する
- 切除不能・再発胆道がん治療の新たな選択肢となるか⁉ インライタによる単剤療法が先進医療として進行中
- 切除不能または術後再発胆道がん 「切れ味の良い」FOLFIRINOXの臨床試験開始へ
- 腫瘍を小さくし手術につなげる 切除不能局所進行胆道がんの術前化学療法
- 手術ができれば根治も!肝内胆管がんの治療法
- 安全性と根治性を備えた肝胆膵領域の腹腔鏡下手術
- 肝胆膵がんは患者さんに見合った多様な病態に対する最善の治療選択を
- 今こそ日本発の胆道がんの新治療薬の開発を!



