血縁ドナーによる骨髄移植の成果に迫る 臍帯血移植は、難治性血液がんを救う切り札になり得るか

内田直之さん
日本で臍帯血(さいたいけつ)移植が始まって約20年、医療技術は進化を続け、最大のデメリットとされた「生着不全」の壁が取り除かれた。以前は、骨髄移植の代替的位置付けだった臍帯血移植だが、ここ10年ほどでその実態は確実に変わりつつある。日本最多の臍帯血移植を手がける虎の門病院血液内科部長の内田直之さんに、臍帯血移植の現状と今後について伺った。
移植治療に進むのはどんなときか
血液がんは、大きく言うと、白血病と悪性リンパ腫の2つのカテゴリーに分けられ、それぞれがさらに細分化され、治療法も個々に異なる。しかし、すべてにおいて言えるのは、薬物療法が効かない場合、もしくは、薬物療法でいったん寛解(かんかい)になったものの再発した場合には、*造血幹細胞移植が適応になるということだ。
そもそも、血液がんにおいて薬物療法が効かないとき、もしくは、いちど寛解に至ったのに再発するとき、体の中では何が起こっているのだろう。虎の門病院血液内科部長の内田直之さんは、白血病を例に、次のように説明する。
「白血病細胞を駆逐するために抗がん薬や分子標的薬を投与したものの叩き切ることができなかった、もしくは、いったん白血病細胞を叩けたように見えたのに実は残っていた、ということです」
正常な血液細胞は、大元になる造血幹細胞が細胞分裂を繰り返して、白血球や赤血球、血小板といった大人の細胞になっていく。これを「分化」というが、遺伝子損傷によって突然現れた白血病細胞は分化できず、未熟な細胞(芽球・がきゅう)のままどんどん増えていく。この芽球が増えた状態を白血病という。
「見た目には同じに見える白血病細胞の中に、芽球に紛れて白血病細胞の親玉となる幹細胞がいることがわかっています。抗がん薬や分子標的薬を投与すると、芽球、つまり雑魚(ざこ)たちはすぐ死滅してくれるけれど、親玉の幹細胞だけは生き残ることがあるのです。そうならないために、抗がん薬治療は、たとえ寛解になっても1コースで終わらせず、3コース繰り返して(地固め療法・じがためりょうほう)、最後に残った白血病幹細胞まできちんと叩くことを目標に行われます」と内田さん。
白血病幹細胞の最後の1つまで叩き切ることができれば「治癒(ちゆ)」。つまり再発はない。ただ、数値的にゼロでも、幹細胞を1つ残らず叩けたかどうかは確認しようがないため、「治癒」ではなく「寛解」と表現されるのだ。もし白血病幹細胞が残っていたら、多くは1年以内、遅くとも2~3年のうちに再発という形で出てくるそうだ。よって、3年たって再発がなければ、「治癒」と考えていいだろう。
話を元に戻そう。薬物療法が効かない、もしくは、一度寛解に至ったのに再発したということは、薬物療法の間もずっとしたたかに生き延びた白血病幹細胞がいた、ということ。つまり、この幹細胞は抗がん薬や分子標的薬から逃れる術を知っており、何度繰り返しても体力を消耗するだけで意味がない。だから次の段階、移植に進みましょう、ということになるのだ。
血縁の骨髄移植が最優先、その次は……
造血幹細胞移植は、他者の骨髄や血液を体内に入れるため、ドナーと患者の血液の性質が合致しなければならない。それを表すのが白血球の型を表すHLA(ヒト白血球抗原)で、骨髄移植の場合、全6座中、願わくば全一致、無理ならば1座のみ不一致の5座一致が条件となる。兄弟姉妹間では4分の1の確率で全一致するため、もともと血縁ドナーからの*骨髄移植が、造血幹細胞移植の始まりだった。
しかし、血縁でドナーが見つからず、非血縁でドナーを探そうとすると、一致の確率は数百から数万分の1と極めて低くなる。その事態を打破すべく1980年代後半から各地で有志による骨髄バンクが作られ、1992年にそれらを統合する形で日本骨髄バンクが立ち上がった。臍帯血移植が始まったのは、それから10年ほど後、1999年に臍帯血バンクができて以降になる。
こうした歴史を経て、造血幹細胞移植には現在、血縁間の骨髄移植(または*末梢血幹細胞移植)、非血縁の骨髄移植(または末梢血幹細胞移植)、そして臍帯血移植の3つの方法がある。では、いざ移植となったとき、どの方法が優先的に選択されるのか。長きにわたって、まずは血縁ドナーによる骨髄移植(もしくは末梢血幹細胞移植)が最優先。血縁にドナーが見つからない場合は、骨髄バンクに登録してドナーを待つ非血縁の骨髄移植、それが難しい場合に臍帯血移植、という順番で移植法が選ばれてきた。ところが、ここ10年ほどで実情が変わってきているらしい(図1)。
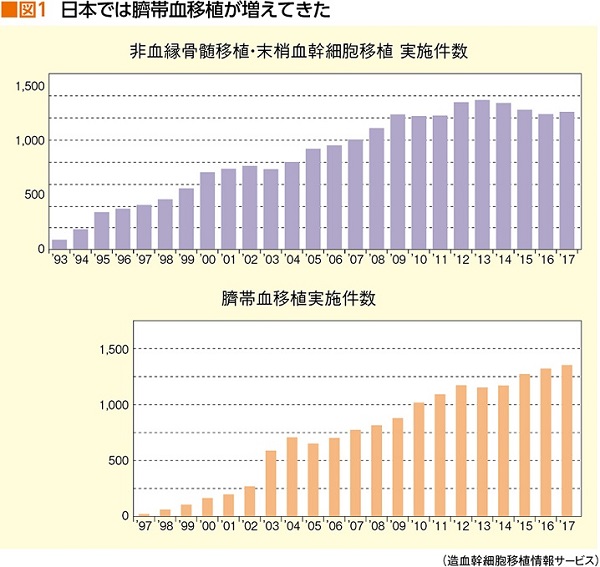
「血縁ドナーが見つかれば、第1選択は今も血縁ドナーによる骨髄移植か末梢血幹細胞移植が多いと思います。ただ、血縁ドナーが見つからない場合の第2選択肢は、骨髄バンクに登録して半年近く待たなくてはならない非血縁の骨髄移植ではなく、臍帯血移植に進むようになってきました」と内田さんは指摘する。
臍帯血移植が始まって約20年、始めの10数年は「生着不全が多い」というデメリットがあったそうだ。「生着」は移植にとって山場であると当時にスタート地点。生着できないとは、移植のスタートを切れないことを意味した。当時の臍帯血移植の生着率は70~80%。10人に2人~3人は生着できなかったことになる。これが3つの移植法の中で臍帯血移植が3番手に位置し、積極的に選ばれてこなかった最大の理由だ。
ところが現在、医学の進歩でこの数字は飛躍的に上昇。虎の門病院の臍帯血移植の生着率は、すでに2011年から2013年の200例について、99%という数字を叩き出している。全国的に見ても、90%は優に越えているそうだ。
「HLA完全一致の血縁ドナーからの骨髄移植(もしくは末梢血幹細胞移植)の場合はほぼ100%生着するので、その牙城はなかなか崩せませんが、非血縁(骨髄バンク)の生着率95%に比べて、臍帯血移植の生着率は決して劣りません。もはや、生着不全は臍帯血移植のデメリットではなくなりました」
ただ、生着するまでの期間については、骨髄移植の2週間に比べ、臍帯血移植は平均3週間なので、移植から生着までに少々時間を有することは追記しておく。
*造血幹細胞移植=血液細胞を作り出せる細胞を造血幹細胞といい、主に骨髄の中に存在する。正常な血液を作れなくなった患者に、他者(ドナー)の造血幹細胞を入れて新たに正常な血液細胞を作れるように促す治療を造血幹細胞移植といい、骨髄移植、末梢血幹細胞移植、臍帯血移植の3方法がある。
*骨髄移植=造血幹細胞を持つ骨髄液をドナーの腰骨から採取し、患者に移植する治療法。患者のみならず、ドナーの負担も大きい。
*末梢血幹細胞移植=ドナーの骨髄の中にある造血幹細胞をG-CSFという薬剤で刺激することにより血液中に流出させ、それを特殊な採血方法で採取し、患者に移植する治療法。
臍帯血移植の仕組みと手順
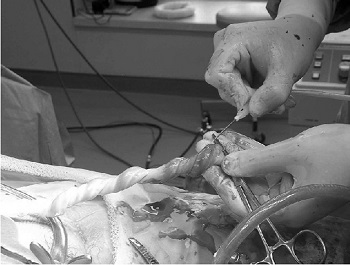
ここで、臍帯血移植について詳しく見てみよう。
臍帯血移植の「臍帯」とはへその緒。お母さんのお腹の中にいるとき、赤ちゃんは、へその緒を通して栄養を受け取っているが、生まれると同時に母乳やミルクを口から摂取するようになるため、へその緒は不要となり破棄される。
ところが、そのへその緒には、血液を作り出す源となる造血幹細胞が豊富に含まれた血液が詰まっていることが、1982年に明らかになった。これを機に、研究が重ねられ、産まれたばかりの赤ちゃんの臍帯から造血幹細胞を取り出して、正常な血液を作ることができない人に移植する治療法が確立された。これが臍帯血移植である(写真2)。
1997年に日本初の臍帯血移植が成功。1999年の公的臍帯血バンク立ち上げを機に、日本でも本格的にスタートした。現在、臍帯血バンクには常に1万ほどの臍帯血が常備されているという。6座あるHLAのうち、臍帯血移植では2座不一致まで移植可能なため、1万の常備で臍帯血移植希望者のニーズほぼ全てに応えられるそうだ。
臍帯血移植の手順は、基本的には骨髄移植と同じ。まず、白血球をゼロにするための移植前治療を行う。1週間かけて大量の抗がん薬投与と放射線治療を行い、白血病細胞をできる限り叩くと同時に、患者自身の免疫細胞も叩き、白血球をすべて排除する。大量抗がん薬投与による口内炎、下痢、食欲低下、脱毛といった副作用は、投与終了間際から一気に始まることが多く、これが第1の山場だ。
2番目の山場は、1番目の山を越え、白血球の値がゼロになっている期間での副作用。水様性の下痢や口内炎はもちろん、いちばん怖いのは肺炎や敗血病など感染症だ。白血球ゼロの状態とは免疫力が全くないことを意味し、ちょっとした感染症が命取りになる。臍帯血移植は、白血球がゼロになっているこの期間に行われる。移植自体は、20ccの臍帯血を静脈注射で投与するだけなので、ものの5分ほどで終わるそうだ。そこから、ドナーの造血幹細胞が分化して白血球が増えてくる(生着)までに約3週間。この期間は白血球ゼロの状態が続くため、さまざまな副作用に耐えながら、常在菌を含め、細菌やウイルスに接触しないよう、無菌室で過ごすことになる。
移植から3週間、いよいよ新しい白血球が増えてきたときが「生着」だ。そして、生着を喜ぶ間もなくやってくるのがGVHD(移植片対宿主病)。生着した新しい白血球が、自身以外の細胞を「異物」と見なし、攻撃し始めるのだ。その症状は皮疹、下痢、肝臓細胞破壊による黄疸など重篤(じゅうとく)、かつ多岐にわたる。ときに命を落とすこともあるため、厳重な管理が必要だ。これが第3の山場で、2カ月から3カ月ほど続く。
GVHDの症状が落ち着くまでに、順調にいけば約2カ月間。ここを乗り越えたら、ひとまず「移植成功」となるが、表現としては、やはり「寛解」になるそうだ。
「薬物療法でも、移植でも、重要なのは、白血病の幹細胞を1つ残らず排除できたかどうかです。抗がん薬を大量投与してもなお、生き残ってしまう白血病の幹細胞があります。でも、たとえ抗がん薬では叩き切れなくても、移植で体内に入ってくるのは他者の白血球。この白血球は〝異物〟と見なしたものをことごとく攻撃するのですから、当然、白血病幹細胞も攻撃します。新しい白血球の攻撃によって白血病幹細胞が完璧に体から排除されることを期待し、叩きのめしてくれ、と願いながら移植治療をするわけです。移植終了後、1年、2年、3年が過ぎて再発しなければ、晴れて〝治癒〟と言っていいでしょう」
これをGVL効果(移植片対白血病効果)という。つまり、GVHDとGVLはどちらも、新しい白血球の異物攻撃が生み出す背中合わせの状態と言えるだろうか。GVHDが強ければGVLも強いと言えることから、ある程度強いGVHDは白血病細胞撃退のために必要なことでもあるのだ。ちなみに、「移植して寛解した後も、万が一、白血病幹細胞が残っていたら、ほとんどが1年以内、遅くとも2年以内に再発します」と内田さん。2年経てばほぼ大丈夫。ごくまれに3年目に再発することがあるので、完全に治ったと判断できるのは移植後3年が過ぎたときだという。
同じカテゴリーの最新記事
- ドナー不足を一気に解消したHLA半合致移植と移植後GVHDの新薬 白血病に対する造血幹細胞移植の最新情報
- 分子標的薬やCAR-T細胞療法などの開発で全ての血液がんに希望が 分子標的薬の新薬、次々登場で進化する血液がんの化学療法
- 日本血液学会が『造血器腫瘍ゲノム検査ガイドライン』を作成 「遺伝子パネル検査」によりゲノム情報は、血液がんの正確な診断・治療に必須
- 白血病に対する新しい薬物・免疫細胞療法 がん治療の画期的な治療法として注目を集めるCAR-T細胞療法
- 血液がんの上手な日常での副作用管理 感染症対策が最重要。骨髄移植した患者はとくに注意を!
- 治療が長引く可能性も 血液がん患者の口腔ケアはセルフケアと専門医とのタッグが重要
- 造血幹細胞移植患者のリハビリは「継続する」ことが大切
- “不治の病”とされていた血液がん。治療法の進歩で、治癒が目指せるがんへ これだけは知っておきたい! 血液がんの基礎知識 白血病編
- 「不治の病」から「治癒可能な病」になったが、まだまだあなどれない これだけは知っておきたい白血病の基礎知識



