日本血液学会が『造血器腫瘍ゲノム検査ガイドライン』を作成 「遺伝子パネル検査」によりゲノム情報は、血液がんの正確な診断・治療に必須

造血器腫瘍(血液がん)では、遺伝子の異常が治療の選択には必須であることが強く認識され、今までにも染色体検査やFISH法などさまざまな方法で、遺伝子の異常を検出し診断・治療につなげてきた。2018年5月、日本血液学会は、次世代シークエンス(NGS)の技術を有効に活用すべく、『造血器腫瘍ゲノム検査ガイドライン』を作成した。ガイドライン作成の部会長、京都大学医学部病理学第二講座教授の小川誠司さんにその概要を伺った。
「ゲノム検査」とは
「ゲノム」とは生物が持つ染色体のなかにある総てのDNA配列情報のことで、ゲノム解析技術の急速な進歩により、がんについてはここ数年で実に多くのことが解明され続けてきた。分子標的薬や免疫チェックポイント阻害薬など、さまざまなタイプの新薬の開発と相まって、今後も、適切な診断と治療の細分化がますます進んでいくことが期待されている。
なかでも造血器腫瘍(血液がん)は、種類が非常に多く多岐にわたる疾患で、確定診断のために以前からさまざまな遺伝子異常を突き止めて治療につなげるという点で、他の固形がんよりも進んでいるがん種だった(図1)。
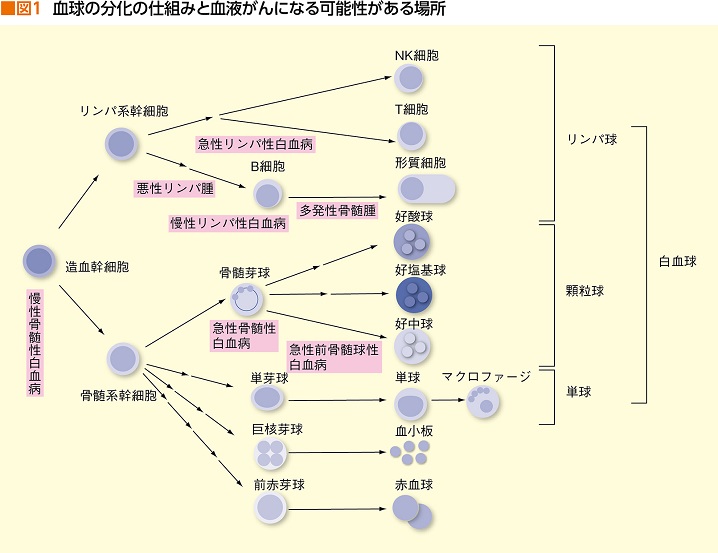
今では、あらゆるがんの標準治療にもなってきた分子標的薬についても、固形がんに先んじてさまざまな研究がなされ、グリベック(一般名イマチニブ)が2000年に登場し大成功を収めた。たとえ分子標的薬がなくても、血液がんにとっては正確な診断には遺伝子検査は必須だった。
そんな中、近年、ヒトのDNAの塩基配列を高速で読み出せる次世代シークエンサー(Next Generation Sequencer:NGS)が注目されている。
次世代シークエンサーは、限定的な目的に対してではなく、1度の検査で網羅的に遺伝子異常を見つけることができる検査法だ(遺伝子パネル検査)。
現在、先進医療が実施され、来年(2019年)保険適応とする方針が厚労省から示されていて、NCCオンコパネル(国立がん研究センター中央病院)、TodaiOncoPanel(東大)、OncoPrime(京大、千葉大他)、OncomineAsssay(岡大、九大他)などがある。
ただし、現状ではこの遺伝子パネル検査は固形がんで全身に転移したり、希少がん、原発不明がんなどに限られており、114の遺伝子と13の融合遺伝子に対してという、限られた遺伝子に対しての検査である。
ゲノム検査は分子標的薬の選択には重要だが、その1つでしかない
血液がんについては、日本血液学会が、遺伝子パネル検査を念頭に置きつつ、近い将来、薬事承認、保険収載を目指しながら、その一方では、将来的には、WGS(Whole Genome Sequencing)という次世代シークエンサーを用いて、全ゲノム領域を解読する最も包括的な手法や、WES(Whole Exome Sequencing)という次世代シークエンサーを用いて、ほぼすべての遺伝子のタンパクをコードするゲノム領域を解読する方法を臨床導入するという方向性も見据えている。
「次世代シークエンスのメリットは、治療の選択肢を細分化して、最良の治療を適切に決めることができる可能性がある点ですから、ただ単に、分子標的薬を適応できるかどうかということだけを目的とするのは短絡的な考え方と言えます。
遺伝子を調べて特定の薬の可能性を見つけるというのは、ほんの一部の意義なのです。もちろん、重要な一部ではありますが、それだけを目指すのでは、広い視野を欠いていると言わざるを得ません。そういう方向性に進んでいくことに対して、私はとても懸念しています」と小川さんは話す。
さらに、分子標的薬だけにフォーカスしすぎて、重要な情報を十分に調べることをしないと、多くの患者が適切な治療を受けるという恩恵を得られなくなる可能性があるという。
ゲノム医療に対する基本的な考え方を提供
そして、日本血液学会では、遺伝子検査の結果がより正しく利用されるようにある種の指針(ガイトライン)が必要であると考え、2017年8月にゲノム医療部会を発足した。その後、わずか9カ月後の2018年5月に、『造血器腫瘍ゲノム検査ガイドライン』を策定した。
今後、臨床導入が予想される「遺伝子パネル検査」の基盤となる遺伝子群を提案すると同時に、がんゲノム医療に対する基本的な考え方を提供するものだ。
『造血器腫瘍ゲノム検査ガイドライン』は、網羅的に遺伝子をAからZまで分類し、まず、目次的な一覧表から、個々の遺伝子にアクセスすることができるようになっている。そして、それぞれの遺伝子について、「遺伝子変異について該当する造血器腫瘍」「臨床的有用性」「遺伝子変異の機能的意義とその種類」「関連する染色体構造変化」「エビデンスレベル(診断・治療・予後)」「薬剤」というそれぞれの項目において、現時点で解明されていることが記入されている。
そして、一般の臨床医が知識のアップデートをはかるということのみならず、血液がんの患者やその家族など、一般の人々も閲覧できるように、わかりやすいレファレンス(検索・参照)機能を持たせている。
エビデンス(科学的根拠)レベルとその評価についての解説、腫瘍の略称の説明なども載っており、日本血液学会のホームページからアクセスすることができる(画像)。
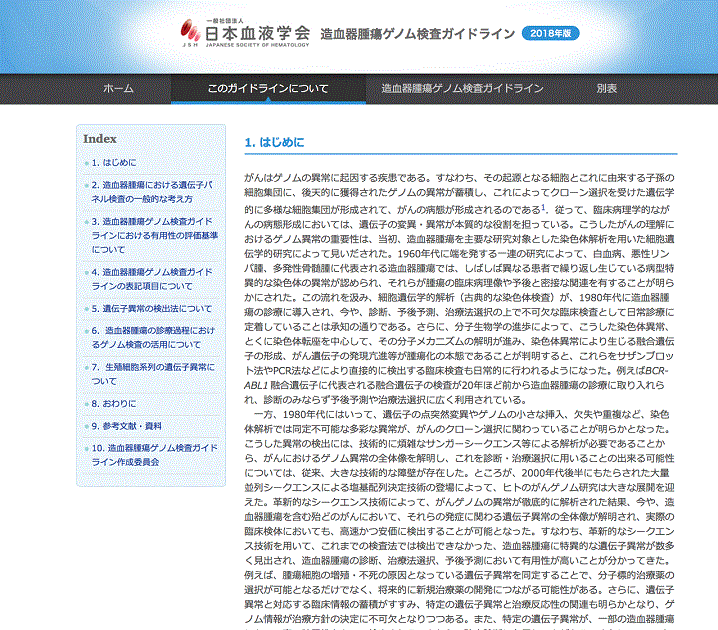
例えば、ABL1という遺伝子に関する情報を閲覧すると、同じABL1のページは、6つに分かれているが、そのなかの1つでは、該当する造血器腫瘍は、慢性骨髄性白血病(CML)で、臨床的有用性はグレード1(臨床的有用性が高い遺伝子異常)。遺伝子変異の機能的意義とその種類は、機能獲得(融合:BCR/ABL1)で、関連する染色体機能構造はt(9;22)(q34;q11)。
エビデンスレベルは診断A、治療A、予後A。(それぞれの根拠となる論文、学会指針、臨床試験が示されている。ちなみにエビデンスレベルはAからの4段階で最もエビデンスレベルが高い場合がAとなる)
薬剤はグリベック、スプリセル(一般名ダサチニブ)ほかの薬剤が「薬事承認」「FDA(米国食品医薬品局)承認」「臨床試験中」というように分類されていて、それらの情報を1ページのなかで一覧することができるのだ。
この例のように、すべての項目に対して情報が埋まっている遺伝子は、現時点ではきわめて少ない。しかし、今後の臨床研究によって少しずつ解明され埋まっていくことになるだろう。
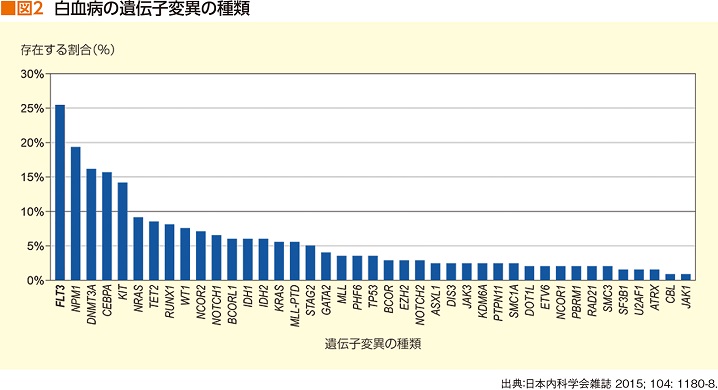
そして、情報が埋まっていくことによって、診断、治療、予後予測が徐々に解明され、治療が進化していくことは間違いないだろう(図2)。
同じカテゴリーの最新記事
- ドナー不足を一気に解消したHLA半合致移植と移植後GVHDの新薬 白血病に対する造血幹細胞移植の最新情報
- 分子標的薬やCAR-T細胞療法などの開発で全ての血液がんに希望が 分子標的薬の新薬、次々登場で進化する血液がんの化学療法
- 血縁ドナーによる骨髄移植の成果に迫る 臍帯血移植は、難治性血液がんを救う切り札になり得るか
- 白血病に対する新しい薬物・免疫細胞療法 がん治療の画期的な治療法として注目を集めるCAR-T細胞療法
- 血液がんの上手な日常での副作用管理 感染症対策が最重要。骨髄移植した患者はとくに注意を!
- 治療が長引く可能性も 血液がん患者の口腔ケアはセルフケアと専門医とのタッグが重要
- 造血幹細胞移植患者のリハビリは「継続する」ことが大切
- “不治の病”とされていた血液がん。治療法の進歩で、治癒が目指せるがんへ これだけは知っておきたい! 血液がんの基礎知識 白血病編
- 「不治の病」から「治癒可能な病」になったが、まだまだあなどれない これだけは知っておきたい白血病の基礎知識



