初めての前向き試験で抗EGFR抗体薬の信頼性が確実に! 進化を続ける切除不能・進行再発大腸がんの薬物療法

進行がんの薬物療法は進化しています。大腸がんも例外ではありません。昨年(2022年)1月、3年ぶりに「大腸癌治療ガイドライン」(第7版)が改訂され、遺伝子変異の有無と原発巣の発生場所が治療選択を左右することが記載されました。ただ、その根拠となるデータはすべて後ろ向き解析によるものです。
その後、日本人を対象にした大規模な前向き試験データが発表され、ガイドライン記載の根拠が立証されました。
そこで、切除不能・進行再発大腸がんに対する最新の薬物療法について、聖マリアンナ医科大学病院腫瘍内科部長/腫瘍センター長の砂川優さんに話を聞きました。
治療前に遺伝子変異を調べるのは?
切除不能・進行再発大腸がんと診断され、薬物療法を行う前に必ず行うことがあります。それは、RAS遺伝子、BRAF遺伝子に変異がないか、そしてMSI-High(高頻度マイクロサテライト不安定性)ではないかを調べる遺伝子検査です。
「これらの遺伝子変異の有無で、1次治療の内容が大きく変わってきますから、薬物療法開始前の3つの遺伝子検査は必須です。RASとBRAF遺伝子は『RASKET-B』という1つのキットで調べられますし、MSI検査にもキットがありますので、今は全国どこの施設でも検査を受けることができます」と、聖マリアンナ医科大学病院腫瘍内科部長/腫瘍センター長の砂川優さん。
MSI-Highについては、進行大腸がんの約3%と頻度は低いものの、該当すれば1次治療から免疫チェックポイント阻害薬(ICI)のキイトルーダ(抗PD-1抗体:一般名ペムブロリズマブ)を使うことができます。さらに2次治療では、オプジーボ(抗PD-1抗体:一般名ニボルマブ)+ヤーボイ(抗CTLA-4抗体:一般名イピリムマブ)併用療法を行うことができます。
免疫チェックポイント阻害薬の恩恵を受けるためにも、薬物療法開始前にはRAS、BRAF遺伝子変異だけでなく、MSIも調べましょう。
発生した大腸がんの場所が重要なのは?
遺伝子変異に加えてもう1つ、薬物療法の治療選択のカギになるのが、「原発巣の発生場所です」と砂川さんは指摘します。
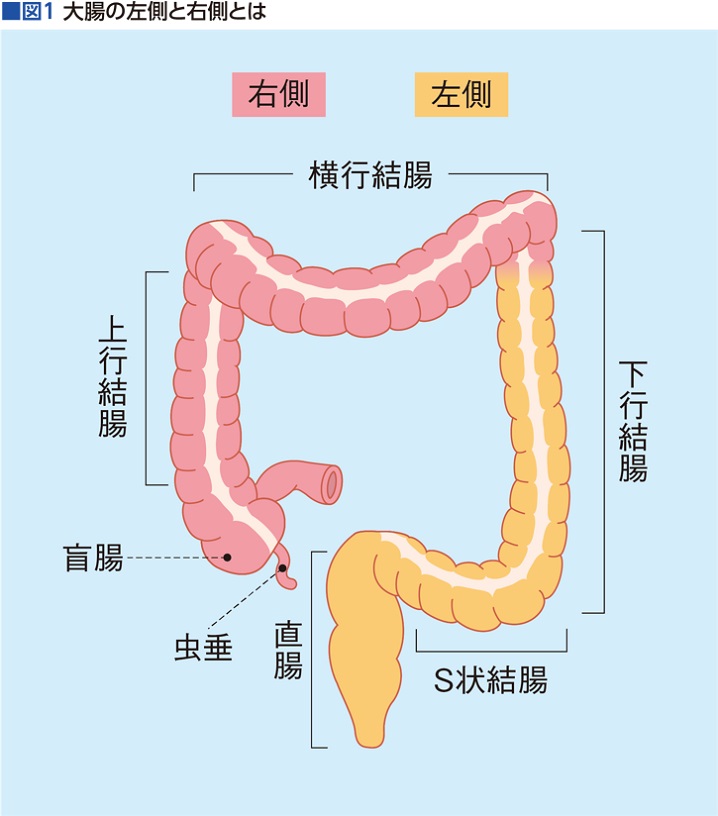
「発生場所が左側(さそく)か右側(うそく)かで、がんの性質が全然違うことが、近年、明らかになってきました。左側と右側とでは生物学的にも発生過程がまったく違うと言われています。右側に発生した大腸がんは、遺伝子変異がたくさん積み重なった〝悪い環境〟から発生するイメージですね。なので、性格も違い、予後が良くないのです」
発生頻度としては、大腸がんのおよそ70%が左側で30%が右側。実は、大腸がんを左右に分けて捉えるようになったのは、ここ10年ほどのことだといいます。
「2012年くらいから、左側、右側という議論が始まりました。当時、海外で『大腸がんは左と右で、予後が全然違うぞ』と言われ始め、遺伝子変異の割合も違うことが発表されました。そこから左右の違いが注目され、臨床試験は左側と右側で分けて解析されるようになり、効果を示す薬剤も違うことがわかってきたのです」(図1)
原発巣左側、RAS/BRAF野生型の1次治療は?
遺伝子変異の有無と腫瘍の発生場所という2つのキーポイントを踏まえて、具体的に、1次治療から見ていきましょう。
RAS遺伝子、BRAF遺伝子ともに変異がない場合(野生型)、原発巣の発生場所が決め手になります。
大腸の左側(直腸、S字結腸、下行結腸)に発生したがんには、*FOLFOX(または*FOLFIRI *FOLFOXIRI)+アービタックス(抗EGFR抗体:一般名セツキシマブ)。アービタックスの代わりにベクティビックス(抗EGFR抗体:一般名パニツムバブ)を使うこともあります。
「RAS/BRAF野生型かつ左側の大腸がんに対する抗EGFR抗体薬の効果は、昨年のガイドライン改定にも表記されましたが、実はその根拠はすべて後ろ向き解析によるものだったのです。それが昨年、前向き試験『PARADIGM試験』の結果が日本から出て、RAS、BRAF野生型かつ左側の大腸がんに抗EGFR抗体薬の使い方の信頼性が増しました」
*FOLFOX:5-FU+レボホリナート+オキサリプラチン併用療法
*FOLFILI:5-FU+レボホリナート+イリノテカン併用療法
*FOLFOXILI:5-FU+レボホリナート+オキサリプラチン+イリノテカン併用療法
原発巣右側、RAS/BRAF野生型の1次治療は?
一方、右側(虫垂、盲腸、上行結腸、横行結腸)に発生した大腸がんには、たとえRAS/BRAF野生型であっても、1次治療は、FOLFOX(またはFOLFIRI、FOLFOXIRI)+アバスチン(一般名ベバシズマブ)となります。
「先に述べたように、右側の大腸がんはそもそも遺伝子変異が積み重なった環境から発生しているので悪性度が高いのです。たとえRAS/BRAF変異がなくても、他の遺伝子変異を複数持っていることが多々あります。そうした性質を持つ右側の大腸がんには、抗EGFR抗体薬は効きにくいのです」と砂川さん。
FOLFOXIRI+アービタックスとアバスチン比較「DEEPER試験」とは?
砂川さんは、今年(2023年)1月、「DEEPER試験」について「ASCO GI 2023」(米国臨床腫瘍学会消化器がんシンポジウム)で発表しました。
「DEEPER試験」とは、原発巣が左側で、RAS/BRAF野生型の進行大腸がん患者さんの1次治療として、FOLFOXIRI+アービタックス群とFOLFOXIRI+アバスチン群を4年間追跡した試験です。
結果は、FOLFOXIRI+アービタックス群の無増悪生存期間(PFS)が有意に延長しました。これによって、原発巣左側でRAS/BRAF野生型の進行大腸がんの1次治療には抗EGFR抗体薬が有効であることが立証されたのです(図2)。
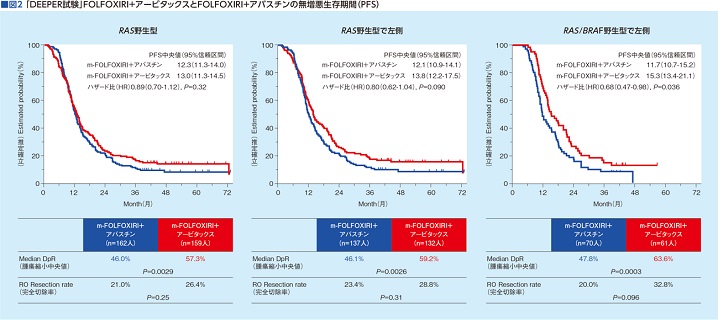
ここで、右側、RAS/BRAF野生型の1次治療について、今回の「ASCO GI 2023」で示された「PARADIGM試験」の新たな見解について砂川さんは言及しました。c「今回、RAS/BRAFに限らず遺伝子変異がない人に対象を絞り込んだ場合、原発巣の左右に関わらず、抗EGFR抗体薬が効果を示すとの結果が示されました」
遺伝子異常が認められなかった場合は、原発巣の左右に関わらず、ベクティビックス群で全生存期間(OS)が延長。OS中央値は、ベクティビックス群41.3カ月vs.アバスチン群34.4カ月。ちなみに、いずれかの遺伝子異常が認められた場合は、ベクティビックス群19.0カ月vs.アバスチン群22.2カ月で、アバスチン群が優位でした。
このことは、RAS/BRAFだけでなく複数の遺伝子すべてに異常がない場合に限っては、右側でも抗EGFR抗体薬が奏効する可能性があることを示唆しています。
「とはいえ、現状は1次治療前に遺伝子パネル検査はできませんし、右側はRAS/BRAFに変異がなくてもその他の変異を持つケースが多いので、やはり血管新生阻害薬アバスチンを選択すべきとの方向性に変わりはないと考えます」(砂川さん)
同じカテゴリーの最新記事
- 「積極的ポリープ摘除術」で大腸全摘の回避を目指す! 代表的な遺伝性大腸がん——リンチ症候群と家族性大腸腺腫症
- 切除可能な直腸がん試験結果に世界が注目も 日本の標準治療は「手術」で変わりなし
- ビタミンDの驚くべき効果がわかってきた 消化管がん手術後の再発・死亡リスクを大幅に減少
- 世界最大規模の画期的研究の一部解析結果が発表 大腸がんの術後補助療法の必要性をctDNAで判断する
- 遺伝子変異と左右どちら側にがんがあるかが、薬剤選択の鍵を握る! 大腸がん薬物療法最前線
- 化学放射線と全身化学療法を術前に行うTNT療法が話題 進行下部直腸がん 手術しないで完治の可能性も!
- 肛門温存の期待高まる最新手術 下部直腸がんTaTME(経肛門的直腸間膜切除術)とは
- 大腸のAI内視鏡画像診断が進化中! 大腸がん診断がより確実に
- 患者さんによりやさしいロボット手術も登場 新しくなった大腸がんの手術と薬物療法



