治癒率の高い子宮体がん 悪性度に応じて治療を考慮
子宮体がんの術後補助化学療法で再発を防ぐ

子宮頸がんよりも年間罹患者数が多い子宮体がんだが、早期の摘出手術と、その後の術後補助化学療法により予後が非常に良いことも特徴だ。手術から術後補助化学療法までを専門家に伺った。
肥満、遅い閉経などもリスクに
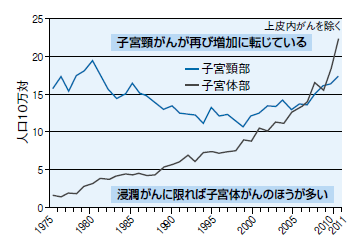
子宮体がんに罹患する患者数は年間で約14,000人と、子宮頸がん(約11,000人)を上回っている。以前は子宮頸がんのほうが圧倒的に多かったが、数年前にその数が逆転した。この状況について、婦人科がんを専門とする慶應義塾大学医学部産婦人科学教室教授の青木大輔さんは「子宮頸がんにかかるのは若い層の女性が多いのですが、子宮体がんは40歳代から大きく増え始めます。日本社会の高齢化とともに、他のがん種と同じく統計学的に増えてきたということです」と話す(図1)。
発生する要因には、女性ホルモンであるエストロゲン(卵胞ホルモン)が関係しているケースが多く、約8割を占めている。子宮内膜の発育を促すエストロゲンの影響が強いと子宮内膜増殖症を経て、子宮体がんが発生することが知られている。肥満、出産経験がない(未経産)、閉経が遅いといった場合に発症のリスクが高まるとされる。
自治体などによる定期検診の項目ではないために、月経不順や不正出血の症状の自覚で受診するケースがほとんどとなる。
子宮体がんの特徴として、早期で発見されれば予後が非常に良いということが挙げられる。実際に比較的早期に発見されることが多く、Ⅰ期(ステージⅠ)が全体の約60%を占める。手術や抗がん薬など治療技術が進歩していることも大きく、Ⅰ期での5年生存率は90%と報告されている。
悪性度と進展度で手術の範囲を決める
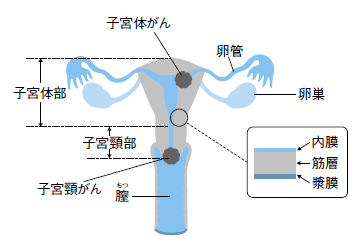
治療は、診断が重要となる。病変部の組織を採取して顕微鏡でがんの悪性度を見て組織学的診断を付けた後に、がんの進展具合を調べるためにCT(コンピュータ断層撮影)、MRI(磁気共鳴画像)を行い、どのくらい広がっているのかを丁寧(ていねい)に調べる(図2)。
青木さんは「筋層浸潤という言葉を使いますが、がんが子宮壁のどれくらいまで浸潤しているかということ(深達度)がかなりダイレクトに予後に結びつくので、その見極めが1つ。そして組織学的分化度の見極めも非常に大事です」と話す。組織学的分化度とは、がんの悪性度を示すもので、高分化型(G1)、中分化型(G2)、低分化型(G3)に分かれる。
「同じ進展具合であってもG3のほうがはるかに予後が悪いため、筋層浸潤の程度などとの組み合わせでどういう治療を行うのかをしっかりと判断します」
治療は、全身への転移のないⅢ期までは手術が圧倒的に多い。子宮と卵管・卵巣を同時に摘出するのが大原則で、がんが筋層まで達して(浸潤して)いれば骨盤のリンパ節の郭清も行う。また、予後の悪いG3や特殊型の場合にはかなり上のほうまで、傍大動脈リンパ節の郭清を行う大きな手術となる。繰り返しになるが、子宮体がんは早期発見が多いため、結果的に手術がそれほど大きくならないケースが多い。
青木さんは「分化度がG1で筋層浸潤がなければ、骨盤リンパ節の郭清は省略しています。骨盤内にとどまる手術では、術後の回復が早く、保険適用もされている腹腔鏡下手術が行われる方向になります。遠隔転移のあるⅣ期についても手術は絶対にしないということではなく、大きな出血を伴っている場合には、止血を兼ねて子宮までは取り、きちんと診断までつけることがあります」と解説する。
悪性度に応じて術後の治療を考慮
手術後はどうするか。早期では治癒率が高く、Ⅰ期では9割を超え、筋層浸潤がなければほぼ100%近いとされている。しかし、進行例であったり、早期でもがんの悪性度が高い場合には再発の可能性があるので、術後補助療法でがんを完全に叩きに行くことになる。治療開始時期は手術からの回復具合などを見て決められるが、「術後1カ月。早ければ早いほどよい」(青木さん)という。
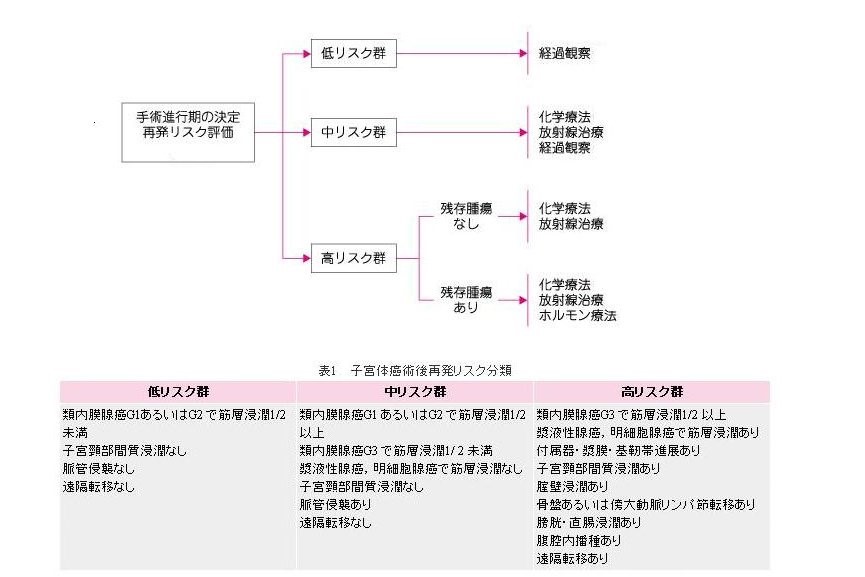
ここでも大切なのはがんの悪性度の見極めだ。再発の危険因子(リスクファクター)の1つである筋層浸潤(深達度)が深いほど再発率が高いし、それにG1~3の分化度などを組み合わせて、術後の追加治療が必要かを判断する。リスクは、低リスク群、中リスク群、高リスク群に分けられ、中リスク群はさらに「low-intermediate群」「high-intermediate群」に細分化される(表1)。
Ⅰ期であっても組織学的分化度がG3であったり、筋層浸潤が1/2を超える(ⅠB期)場合には再発リスクは高まるので、術後補助療法が考慮される(図3)。
欧米では、術後補助療法として放射線による骨盤の治療(骨盤内照射)が主体になる。一方、日本では圧倒的に化学療法が多い。2005年に日本で発表されたランダム化試験(JGOG2033)で、全骨盤照射群と*シクロホスファミド+*アドリアマイシン+*シスプラチン(CAP療法)群を比較した結果、両群間に無再発生存期間(PFS)、全生存期間(OS)ともに差がなく、とくに中高リスクに対しては、化学療法群のほうが再発までの期間が長かったということが示唆されており、その後は放射線治療があまり行われなくなった。
青木さんは「欧米ではリスクの高い症例に対しては、抗がん薬と放射線療法を組み合わせて行っています。放射線単独よりは良いという結果も出つつありますが、日本では高リスクについてもしっかりと抗がん薬を使う。術後に放射線治療を加えると副作用の頻度が増すからです」と化学療法が使われる理由を話す。
*シクロホスファミド=商品名エンドキサン *アドリアマイシン=一般名ドキソルビシン *シスプラチン=商品名ブリプラチン/ランダ
同じカテゴリーの最新記事
- 免疫チェックポイント阻害薬との併用療法で大きく前進 新たな進行期分類が登場した子宮体がんの現在
- 第75回日本産科婦人科学会 報告 ~慈しみの心とすぐれた手技をもって診療に努める(慈心妙手)が今年のテーマ~
- 不正出血を見逃さないで! 子宮頸がんを抜き、増加している子宮体がん
- 症例数はまだ少ないが、高齢者や併存症を持つ患者にも対応可能 子宮体がんにおける重粒子線療法の今
- 子宮体がんの最新治療と今後の可能性 免疫チェックポイント阻害薬を用いた治療が本格的にスタート!
- 子宮体がん、子宮頸がんにおけるダヴィンチ手術の現状と今後 子宮体がんがダヴィンチ手術の保険適用に
- 子宮頸がんはアバスチンを加えた3薬剤、子宮体がんではダヴィンチ、卵巣がんには新薬リムパーザが
- 根治性、安全性、低侵襲性実現のために様々な術式を開発、施行 婦人科がん手術の現状
- 子宮体がんの治療は遺伝子診断による個別化治療へ



