- ホーム >
- 薬 >
- 免疫チェックポイント阻害薬
胃がん新ガイドライン「条件付き承認」で増える治療選択 1次治療でオプジーボ承認

2021年11月、免疫チェックポイント阻害薬オプジーボが、治癒切除不能なHER2陰性の進行・再発胃がんに適応拡大された。3次治療以降ではすでに承認されていたが、それに1次治療も追加となった形だ。これを受けて12月、日本胃癌学会ガイドライン委員会は速報を出し、HER2陰性の1次治療におけるオプジーボの望ましい投与方法についてコメントを発表した。
今回は2021年7月に改定の『胃癌治療ガイドライン医師用第6版』の変更点を含めて、岐阜大学医学部付属病院がんセンター副センター長の牧山明資(あきたか)さんに胃がんの薬物最新治療について伺った。
1次治療でのオプジーボ併用が承認
まず、免疫チェックポイント阻害薬オプジーボ(一般名ニボルマブ)の適応拡大について見ていこう。
抗PD-1抗体薬オプジーボは日本では2017年9月、「がん化学療法後に増悪した治癒切除不能な進行・再発の胃がん」に保険適用され、第5版のガイドラインには3次治療で推奨されるレジメン(治療計画)として記載されている。これが今回、*1HER2陰性の1次治療にも適応拡大されたわけだが、その内容について岐阜大学医学部付属病院がんセンター副センター長の牧山明資さんは言う。
「CPSというバイオマーカーが治療の効果と関係するため、1次治療前にその検査をすることが望ましく、CPSが5以上の人に積極的に推奨するとなっています。しかし、5未満や検査ができなかった患者さんにも、『全身状態や後治療への移行可能性などを考慮して、有効性とオプジーボ併用による副作用増加について十分説明を行った上で、化学療法単独の選択肢も含めて1次治療でのオプジーボ併用を検討することが望ましい』となっていて、5以上なら推奨で、5未満でも使用可能と解釈することが可能です。なぜこのような玉虫色の表現になったかというと『CheckMate 649』という臨床試験の結果でした」
CPSとは腫瘍細胞中や腫瘍内に浸潤した免疫細胞に、オプジーボのターゲットとなるタンパク質PD-L1陽性の細胞がどれくらい含まれているかを見る指標(図1)。

「CheckMate 649試験」は日本を含む全世界で実施された第Ⅲ相試験で、HER2陽性を除く切除不能な進行・再発胃がん・胃食道接合部がん、食道腺がんに対する1次治療として、①*2抗がん薬オキサリプラチンを含む化学療法②同化学療法にオプジーボを併用③抗CTLA-4抗体薬ヤーボイ(一般名イピリムマブ)+オプジーボの3群が比較された。
しかし、途中で③は登録が中止され、1,581例が①化学療法(chemo)群と②オプジーボ+化学療法(NIBO+chemo)群に割り付けられた。主要評価項目はCPS5以上における無増悪生存期間(PFS)と全生存期間(OS)だった。
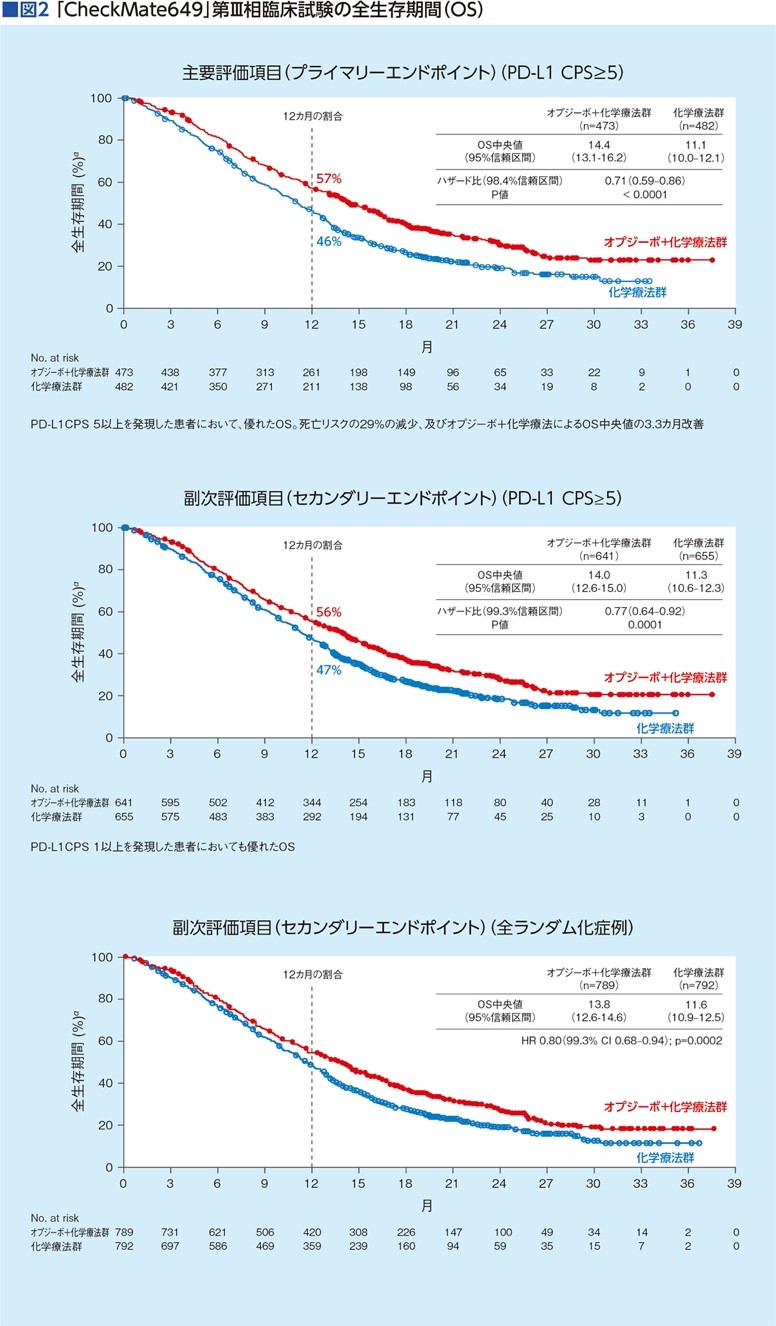
結果はCPS5以上でPFSが優位に延長し(中央値①6.1カ月 vs. ②7.7カ月)、奏効割合も①45% vs. ②60%とオプジーボ併用群で高かった。また、OSも併用群が延長していた(中央値①11.1カ月 vs. ②14.4カ月)。
しかも、CPS5以上におけるグレード3以上の有害事象は①44% vs. ②59%で、「オプジーボはOSとPFSを延長し、許容できる安全性プロファイルを示した初めてのPD-1阻害薬」となった(図2)。
*1 がんの増殖に関係するタンパク質で、がん細胞の表面に多く存在しているとHER2陽性、存在していないとHER2陰性と呼ぶ。これをターゲットにした抗HER2薬にはハーセプチン(一般名トラスツズマブ)がある
*2 CapeOX療法(カペシタビン+オキサリプラチン)またはFOLFOX療法(5-FU:一般名フルオロウラシル+レボホリナート+オキサリプラチン)
状態の悪い患者さんにこそ1次治療にオプジーボ
その一方、副次評価項目であるCPS1以上やCPS1未満を含んだ全登録例においても、有意なOSの延長が示された。つまり、CPS5未満でも効果があるのではないか、それなら全例で使えばいいのではということになる。ここを明確にするために行われたサブ解析の結果が参考になると牧山さんは言う。
「CPS5以上では*3ハザード比が最小。CPS5以上の人にオプジーボの併用効果が高いことは間違いありません。しかし、CPS5未満や、1未満でもハザード比は1よりも小さく、CPSが低い人にも一定の効果はあると言えます。さらに、1未満、1~5未満、5以上のハザード比を比較した別な解析では、5以上ではハザード比0.7と最も小さいが、1~5未満で0.97、1未満で0.92と、1未満と1~5未満で数値の大小が逆転しています。つまり、1未満には、1~5未満よりも薬剤が効いている人が多く含まれていると推測されます」
「CPSのみで効果の予測は完全ではないですから、CPS5で対象の患者さんを切ってしまうと、恩恵を受けられない人が出る可能性がある。しかも、前者の解析では5未満、1未満でも併用群では生存期間が短縮していません。少なくとも併用して有効性の面で悪さはしないわけです。ガイドライン委員会の速報が『CPS5未満でも状況でオプジーボが使える』としているのはこのためで、おそらく実臨床ではCPSの数値に関わらず、投与することが許容されるだろうと私は考えています」
適用拡大のもとになった臨床試験はもうひとつある。日本、韓国、台湾で実施された第Ⅲ相試験で、HER2陰性の未治療胃がんに対し、標準治療(*4SOX療法またはCapeOX療法)にオプジーボ併用群とプラセボ併用群を比較した「ATTRACTION-4試験」だ。PFSには有意な延長(10.45カ月 vs. 8.34カ月)が示されたが、OSでは示されなかった。
国別のハザード比を見ると、韓国で0.77、台湾で0.78。韓国や台湾の人には効いている一方、日本人では1.04とオプジーボの併用効果を認めないという結果になっている。しかも、プラセボ群の生存期間は19カ月と圧倒的に長い。これはどういうことだろうか(図3)。
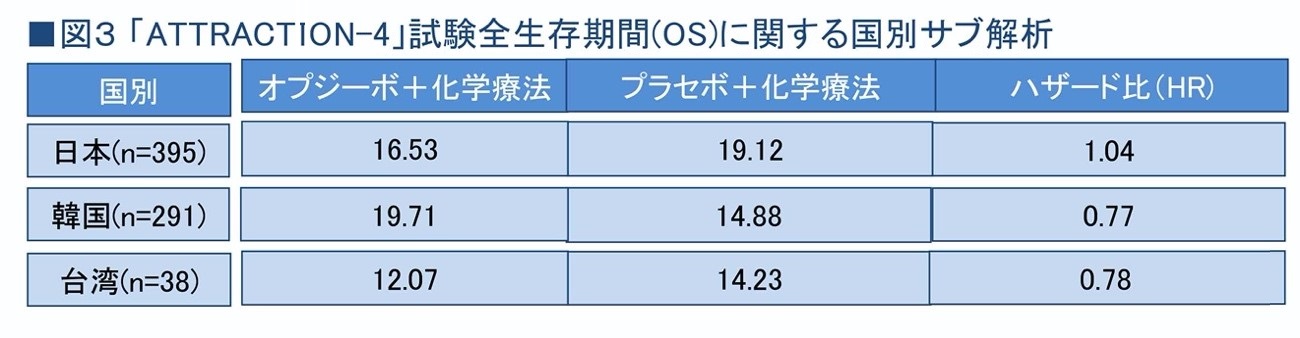
「日本の患者さんの状況をよく見ると、かなりの方が頑張って2次治療を行い、その後の治療で3割弱の方は免疫療法も受けていました。状態のいい患者さんが試験に多く入っており、そのような患者さんでは上乗せ効果が確認しにくかったと推測できます。
しかし、実臨床では後治療に入れない、予後(よご)の悪い患者さんもたくさんいます。状態の悪い患者さんが3次治療まで行えるのはむずかしいことですが、1次治療なら100%の人に届けることができます。実臨床でこそ、オプジーボは早い段階から投与すべきだと考えます。
今後、ガイドライン上での、オプジーボの記載も『1次治療でCPS5以上は化学療法+オプジーボ、5未満で化学療法±オプジーボ、そして1次治療で使われていない場合に3次治療でオプジーボ推奨』となるのではと考えています」
このように、オプジーボの1次治療への適応拡大は、予後のよくない患者さんへの大きな福音といえる。ただし、ひとつ注意点がある。1次治療で免疫にかかわる有害事象が出ると、その後もずっと残る可能性がある点だ。事実、オプジーボ+化学療法群では皮膚毒性、胃腸毒性、肝毒性、過敏症、内分泌障害などの有害事象が確認されている。
「化学療法群と比較するとグレード3以上の有害事象が少し多い印象ですが、極端に多いわけではありません。オプジーボはすでに3次治療以降で使われているので、医療従事者も慣れており、オプジーボ特有の副作用マネジメント体制も病院で確立されていると思います。その体制を生かし、1次治療の有害事象にも備えることが重要と思います」
*3 臨床試験などの指標を客観的に比較する統計方法。A薬とB薬を比べたとき、ハザード比が1なら両薬の効果に差はなく、A薬の数値が小さければ小さいほどA薬のほうが有効と判断される
*4 S-1:テガフール・ギメラシル・オテラシルカリウム+オキサリプラチンの併用療法
同じカテゴリーの最新記事
- 1人ひとりの遺伝子と免疫環境で治癒を目指す! がん免疫治療が進んでいる
- 免疫チェックポイント阻害薬との併用療法で大きく前進 新たな進行期分類が登場した子宮体がんの現在
- 免疫チェックポイント阻害薬で治療中、命に関わることもある副作用の心筋炎に注意を!
- キイトルーダ登場前の時代との比較データから確認 進行性尿路上皮がんの予後が大幅に延長!
- 肺がんに対する免疫チェックポイント阻害薬の治療効果は腸内細菌が関係!
- 複合がん免疫療法が、がん薬物療法の主力に! 免疫療法の個別化医療を目指す
- 乳がん治療にも免疫チェックポイント阻害薬が登場! トリプルネガティブ乳がんで承認、さらに――
- 初期治療から免疫チェックポイント阻害薬選択の時代へ 腎細胞がん治療はここまで来た!
- 患者にもわかりやすく明確化された推奨する治療・しない治療 全面改訂された「大腸癌治療ガイドライン」2019年版



