骨髄異形成症候群(MDS)の正体を知ろう 高リスクの骨髄異形成症候群にはビダーザが決定打。今後の新薬承認に期待

低リスクと高リスクでは、治療法も心構えも違う骨髄異形成症候群(MDS)。いずれも、完治には造血幹細胞移植しか方法はないが、年齢や状況的に移植を受けられないことも多い。今のところ、高リスクの決定打はビダーザだけだが、今後、RAS遺伝子にピンポイントで作用する分子標的薬が出てくる可能性があるそうだ。
骨髄異形成症候群は「がん」なのか?
骨髄異形成症候群(MDS)とはいったい何なのか。そこから話を始めよう。
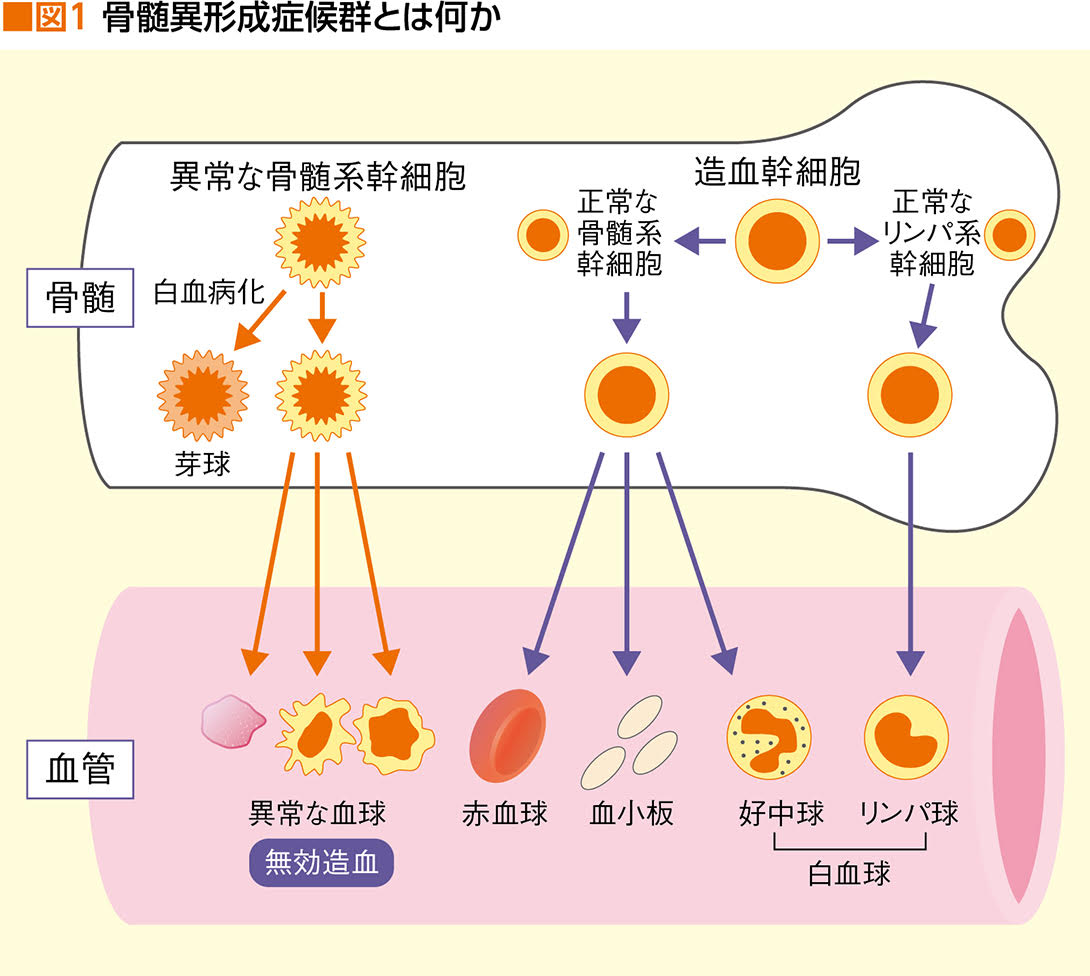
我々の血液には、赤血球、白血球、血小板といった血液細胞(血球)があり、それらはすべて、おおもととなる造血幹細胞から分化して作られる。すべての出発点である造血幹細胞が、まず初めに骨髄系幹細胞とリンパ系幹細胞に分化し、そこからさらに分化を繰り返して、血液細胞になっていくわけだが、その第1段階である骨髄系幹細胞のときに細胞内の遺伝子に何らかの原因で傷がついてしまうと、正常な血液細胞を作ることができなくなっていく。これを骨髄異形成症候群という。
「骨髄を血液生産工場に例えると、工場はフル稼働して血液を作っているのに、できあがるものは不良品(異常な血液細胞)ばかりという状態に陥ってしまうのです。形がいびつだったり、壊れやすかったり、正常な働きができなかったり。これを無効造血といいます」
そう語るのは、がん研有明病院血液腫瘍科部長の照井康仁さん。
それらは芽球(がきゅう:血液細胞になれなかった不良品=白血病細胞)となり、工場(骨髄)から出ていけずに息絶えること(細胞死=アポトーシス)も多いが、血中に出ていったとしても、正常な血液細胞の働きをすることはできない不良品。こうして、血中には不良品ばかりが増え、赤血球、白血球、血小板といった正常な血液細胞は、ジワジワと減っていく。もとはたった1つの骨髄系幹細胞に起こった遺伝子異常から、時間をかけて体全体の血液細胞が減少していくわけだ(図1)。
「以前は、〝白血病の前段階〟などと言われていましたが、病気の発症メカニズム(機序)を見る限り、骨髄異形成症候群も血液がんの1種と認識したほうがいいと思います」と照井さん。
ならば、なぜ「がん」と言わないのかというと、白血病には「骨髄内の芽球が20%以上」という定義があるからだ。そのため、メカニズムとしては白血病と同じだが、骨髄内の芽球が20%未満の状態を「骨髄異形成症候群」と総称するわけだ。
つまり、骨髄異形成症候群は、骨髄系幹細胞の時点で遺伝子に傷を負ったことが原因の「血液のがん」。骨髄内の芽球が20%未満の状態を「骨髄異形成症候群」、20%を越えると「急性骨髄性白血病(AML)」という名前に切り替わる、と捉えてほしい。
高齢者に多く、抗がん薬治療も原因に
骨髄異形成症候群は、もともと高齢者の病気と言われてきた。年齢を重ねるごとに細胞分化の回数も増えるため、骨髄系幹細胞の遺伝子に傷がつく確率も増す、ということが考えられるわけだが、それとともに、老化で遺伝子そのものが不安定になり、傷つきやすくなることもあるそうだ。
また、皮肉なことに、がん治療のための抗がん薬治療も、骨髄異形成症候群を引き起こす要因になっている。強い抗がん薬治療を受けた後、5年~10年を経て骨髄異形成症候群を発症する人が少なくないそうなのだ。
「以前は放射線治療も要因の1つと言われてきましたが、治療で使う放射線量ならば考えなくていいと思います。ただ、原爆被爆は大いに関係あります。広島と長崎に骨髄異形成症候群の患者さんが多いのは偶然ではありません」と照井さんは語る。
骨髄異形成症候群を完治させる方法は、唯一、造血幹細胞移植だけだという。しかし、そもそも高齢者に多く、抗がん薬治療を経たがんサバイバーに多い病気。状況的に造血幹細胞移植が困難である場合が非常に多い。もちろん、コンディションが整うならば、第1選択肢は造血幹細胞移植だ。しかし、それが叶わぬ場合の治療法について、ここから見ていこうと思う。
5q-症候群にはレブラミド
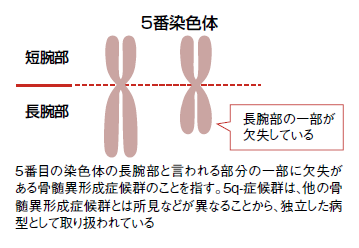
骨髄異形成症候群は、血液検査と骨髄検査を経て確定診断されるわけだが、骨髄検査で採取した骨髄液で染色体検査も行われる。人間には46本の染色体があり、骨髄異形成症候群の中には、5番目の染色体の長腕部(5q)に欠失が起きているタイプがあって「5q-(ファイブ・キュー・マイナス)症候群」と名づけられている(図2)。
症状やリスク段階が幅広く、治療法の選択が難しい骨髄異形成症候群において、5q-症候群だけは、遺伝子のどこに何が起こっているかが明確で、治療法が確立している。かつ、比較的予後(よご)がよいものが多いそうだ。確定診断と同時に判明するので、まずは5q-症候群の治療について触れておく。
治療薬は*レブラミド。「これはがん細胞を攻撃するのではなく、免疫力を高めることでがん細胞にアプローチする免疫調整薬の1種です。1990年代に難治性骨髄腫(なんちせいこつずいしゅ)に使われていたサリドマイドと作用機序は同じですが、サリドマイドの効果を高めるように、かつ副作用を小さくするよう構造を変えた薬です」と照井さんは説明する。
5q-症候群の骨髄異形成症候群に対してレブラミドは明らかに奏功し、2010年に承認された。免疫からアプローチするということで、骨髄異形成症候群全体に効果があるのではないかと期待され、臨床試験が何年も繰り返されてきたが、残念ながら結果は出ていないとのこと。よって現時点では5q-症候群のみに適応されている。ただし、5q-症候群は欧米人には比較的多いものの、日本人には極めて少ないそうだ。
*レブラミド=一般名レナリドミド
低リスクの治療法は、経過観察と支持療法
さて、ここからは、一筋縄ではいかない「骨髄異形成症候群」の治療法について述べていく。「症候群」と言うだけあって、リスク段階も幅広いのが骨髄異形成症候群。低リスクと高リスクでは、同じ病気とは思えないほどの違いがある。
血液検査と骨髄検査を経て「骨髄異形成症候群」の診断がつき、「5q-症候群」でなかった場合、まずは、リスク分類を明確にして、いまの病態がどの位置にあるかを見極めることが重要になる。その指標となるのが、骨髄異形成症候群の予後を予測するIPSS(International Prognostic Scoring System:国際予後判定システム)。
骨髄中の芽球の割合、染色体異常、血球減少の程度を点数化し、その時点での状態を、低リスク、中間リスク1、中間リスク2、高リスクの4段階に分類する。その上で、低リスクと中間リスク1を「低リスク群」、中間リスク2と高リスクを「高リスク群」と考えるそうだ。指標にはIPSSとIPSS-R(改訂IPSS)があって、IPSS-Rは血球減少についての項目が詳しくなり、赤血球、白血球、血小板を個別に見るそうだが、「診断の際は、両方を照らし合わせて判断し、1人ひとりの状態に即して治療戦略を立てます」と照井さんは語る(図3)。

低リスクと高リスクで大きく違うのは「治療介入の仕方」だそうだ。低リスクならば、骨髄中の芽球5%あたりで何年も通常と変わらない生活を続けることができる場合も多く、様子を見ながら、必要に応じて輸血などの支持療法を行っていく。ところが高リスクになると、放っておくと1年以内に骨髄中の芽球が20%を超えて、あっという間に白血病に進行してしまうので、スピードをもって対応しなくてはならない。低リスクと高リスクでは、治療法から心構えまで、全く違ってくるそうだ。
「低リスクの治療は、血中に正常な血液細胞を補うことが主たる目的になります」と照井さん。血中に不良品の血液細胞が増えて、正常な血液細胞が減ってくると、赤血球不足だと貧血、白血球不足だと感染症や発熱、血小板不足だと出血といった症状が出始める。
こうした症状に対しては輸血で正常な血液細胞を補うわけだが、輸血を続けていくと、体内に鉄が溜まり過ぎ、心臓や肝臓に負担をかけて障害を起こしてしまうことがある。ときには心不全や肝硬変といった命に関わる事態にも陥りかねないので、細心の注意が必要だ。
できれば輸血をしたくない、せめて輸血の回数を減らしたい、ということで着目したのが、エリスロポエチンという腎臓のホルモンだ。エリスロポエチンは腎臓で作られる造血因子で、赤血球の産生を促す。そこで、このエリスロポエチンを細胞レベルから作り出し、さらに実際のエリスロポエチンと同じように赤血球の産生を促すよう遺伝子を組み換えた。そして誕生した薬が*ネスプだ。2014年末に承認以降、骨髄異形成症候群に伴う貧血に使えるようになり、輸血量を減らすことができるようになったそうだ。
「輸血を長く続けることは、体へのリスクが大きい」と照井さんは言う。正常な血液細胞を増やすのに、最も手っ取り早い方法は輸血である。けれども、輸血に伴う鉄過剰症や感染症のリスクを考えると輸血は最小限に抑えたほうがいい、というのが照井さんの考えだ。ちなみに、輸血で鉄が増えすぎた場合は、今も鉄キレート剤である*エクジェイドや*ジャドニュによる除鉄療法で対応するそうだ。
*ネスプ=一般名ダルベポエチン アルファ *エクジェイド=一般名デフェラシロクス *ジャドニュ=一般名デフェラシロクス
同じカテゴリーの最新記事
- 免疫チェックポイント阻害薬の2剤併用療法が登場 肝細胞がんの最新動向と薬物療法最前線
- 新薬や免疫チェックポイント阻害薬も1次治療から 胃がんと診断されたらまずMSI検査を!
- リムパーザとザイティガの併用療法が承認 BRCA遺伝子変異陽性の転移性去勢抵抗性前立腺がん
- 免疫チェックポイント阻害薬で治療中、命に関わることもある副作用の心筋炎に注意を!
- SONIA試験の結果でもCDK4/6阻害薬はやはり1次治療から ホルモン陽性HER2陰性の進行・再発乳がん
- dose-denseTC療法も再脚光を ICI併用療法やADC新薬に期待の卵巣がん
- 心不全などの心血管の副作用に気をつけよう! 乳がんによく使われる抗がん薬
- 新規薬剤の登場でこれまでのサブタイプ別治療が劇的変化! 乳がん薬物療法の最新基礎知識
- 世界最大規模の画期的研究の一部解析結果が発表 大腸がんの術後補助療法の必要性をctDNAで判断する
- 「過剰検査・過剰治療の抑制」と「薬物療法の進歩」 甲状腺がん治療で知っておきたい2つのこと



