抗がん剤の効果と副作用を予測するだけでなく、予後も予測する
個別化医療の実現を可能にするバイオマーカーに大きな期待

埼玉医科大学国際医療センター
臨床腫瘍科・腫瘍内科の
藤田健一さん
バイオマーカーは、抗がん剤の効果と副作用をあらかじめ予測する手段として、今治療現場での応用が進んでいる。
しかし、埼玉医科大学国際医療センター臨床腫瘍科・腫瘍内科で薬学を専門とする藤田健一さんによると、バイオマーカーの利用価値はそれにとどまらないという。藤田さんに、バイオマーカーの現状と展望について聞いた。
効果と副作用の個人差を解明し、大きくクローズアップ
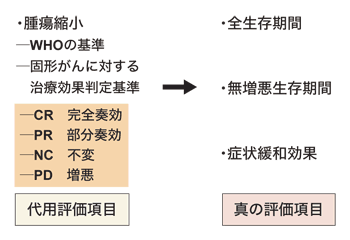
[「殺細胞性抗がん剤が効いていること」の指標]
がん患者にとって、抗がん剤の効果と副作用をあらかじめ予測できたら、というのは切実な願いだ。奏効率を示されても、自分の場合はどうなのか。副作用ばかり強く、効果がないのではないかという不安が、抗がん剤治療に対する患者の恐怖感を誘う原因にもなっている。
ところが、分子標的治療薬の登場をきっかけに、バイオマーカーの存在が大きくクローズアップされるようになった。埼玉医科大学の藤田健一さんによると、バイオマーカーには、薬の効果と副作用を予測する効果予測、がんの悪性度など疾患の経過すなわち予後を予測するという2つの目的があるという。
それらを効果的に用いることによって、最終的には患者それぞれに最適ながんの個別化医療を実現することが期待されている。もっとも、こうした考え方は、分子標的治療薬の登場以前からあったのだそうだ。
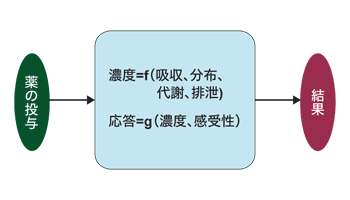
「殺細胞性抗がん剤でも分子標的治療薬でも、効果や副作用には個人差があります。同じ薬を投与しても、体格や年齢、肝臓や腎臓の障害、合併症、過去の治療歴などいろいろな要因で薬に対する反応は異なります。こうした個体差を臨床薬理学では体内での薬物動態と薬力から解明しようとしてきたのです」
薬物動態は体内での薬の動きのことだ。投与された薬は体内で吸収、代謝を受け、移動し、排泄される。それによって、薬の血中濃度が決まる。薬力は体に対する薬の作用のことだ。薬は、作用部位で標的とする細胞の受容体と結合したり、細胞内の情報伝達を阻害するなどして作用する。その結果が、薬の効果や副作用として現れるわけだ。
人体から得られる情報の全てがバイオマーカーになりうる
この薬物動態や薬力に影響して、効果や副作用などの個体差を生むものは何か。遺伝的因子など先天的要因と食事や喫煙などの後天的因子があるという。遺伝的に薬物を代謝する酵素が多いか少ないか、働き方がどうか、喫煙や食事もその過程に影響するのだそうだ。
「この中で、遺伝的な背景を追求するのが薬理遺伝学です。分子標的治療薬だけではなく、殺細胞性抗がん剤でも塩酸イリノテカン(商品名カンプト、トポテシン)のように代謝酵素の遺伝子多型(遺伝子の変異)を調べることで毒性が強く現れるかどうか、わかる薬も出てきました」と藤田さん。 遺伝子多型もバイオマーカーの1つ。バイオマーカーによって効果予測できるのは、分子標的治療薬だけではないのである。分子標的治療薬の登場によって、バイオマーカーがクローズアップされるようになったのは、「分子標的治療薬は、基本的に標的がはっきりしているので、標的が発現しているかいないかなど、バイオマーカーで区別がしやすいからなのです」と藤田さんは説明する。
実際には、画像診断から心電図、骨密度、薬物代謝酵素や受容体の量など、およそ人体から得られる情報の全てがバイオマーカーになりうるという。藤田さんは「要は、その中で、どれがある薬の効果と副作用に関係するかなのです」と話す。
分子標的治療薬の代表的なバイオマーカーはEGFR
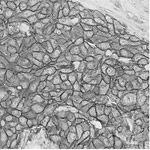
過剰発現しているHER2タンパク。
写真は発現量が強陽性(3+)の細胞例
たとえば、分子標的治療薬の代表的な標的の1つに、EGFR(上皮成長因子受容体)がある。日本で最初に転移性乳がんの分子標的治療薬として認可されたハーセプチン(一般名トラスツヅマブ)も、EGFRの2番、つまりHER2というタンパクをターゲットにした抗体薬だ。
HER2にリガンド(特定のタンパク質や細胞膜の各種受容体などと特異的に結合する物質)が結合すると、チロシンキナーゼ(特定のアミノ酸「チロシン」にリン酸を付加する機能を持った酵素)が活性化されて細胞内の核に情報が伝達され、細胞増殖のスイッチが入る。HER2は、正常の細胞にもあるがその量はわずかだ。
ところが、乳がんの中にはこれが過剰発現しているものが20~30パーセントあり、こういう人は予後が悪いと言われていた。転移性乳がんになると、約40パーセントに過剰発現がある。これは、HER2が過剰発現していると、細胞増殖シグナルが過剰に活性化して、細胞がどんどん分裂・増殖するからと考えられている。
これをブロックするのが、ハーセプチンだ。ハーセプチンはHER2に結合して、リガンドが結合するのをブロックし、細胞増殖のスイッチが入るのを防ぐ。適応の有無をみるバイオマーカーとなるのが、HER2の発現量だ。HER2の発現量が3+か2+かで、奏効率が35パーセント対0と大きく異なる。強陽性(3+)の場合、乳がん再発後の初回治療に化学療法単独よりハーセプチンと併用したほうが、全生存期間が長いことが証明されている。
同じカテゴリーの最新記事
- 有効な分子標的治療を逸しないために! 切除不能進行・再発胃がんに「バイオマーカー検査の手引き」登場
- 正確な診断には遺伝子パネル検査が必須! 遺伝子情報による分類・診断で大きく変わった脳腫瘍
- 高濃度乳房の多い日本人女性には マンモグラフィとエコーの「公正」な乳がん検診を!
- がんゲノム医療をじょうずに受けるために 知っておきたいがん遺伝子パネル検査のこと
- AI支援のコルポスコピ―検査が登場! 子宮頸がん2次検診の精度向上を目指す
- 「尾道方式」でアプローチ! 病診連携と超音波内視鏡を駆使して膵がん早期発見をめざす横浜
- 重要な認定遺伝カウンセラーの役割 がんゲノム医療がますます重要に
- 大腸のAI内視鏡画像診断が進化中! 大腸がん診断がより確実に
- 「遺伝子パネル検査」をいつ行うかも重要 NTRK融合遺伝子陽性の固形がんに2剤目ヴァイトラックビ
- 血液検査で「前がん状態」のチェックが可能に⁉ ――KK-LC-1ワクチン開発も視野に



