患者のためのがんの薬事典
グラン(一般名:フィルグラスチム)
「好中球減少症」を改善し、化学療法をサポートする注射薬

抗がん剤が効いていても、副作用として起こる好中球減少症によって、治療を中断しなければならないことがあります。抗がん剤の減量や、投与スケジュールの変更を余儀なくされることもよくありました。これらの副作用を改善したのが、グランです。
好中球を増やし、好中球の機能を亢進させる作用を持つこの薬は、好中球減少症を改善させることで、がんの化学療法をサポートします。
化学療法の副作用「好中球減少症」を改善
がんの化学療法を受けていると、白血球の一種である好中球が減少し、予定通りに化学療法が行えなくなることがあります。好中球が減少すると、免疫の働きが低下してしまい、感染症にかかる危険性が高まるからです。
こうした化学療法による副作用の好中球減少症を改善したり、防ぐために使われている薬がG-CSF(顆粒球コロニー刺激因子)製剤「グラン」(一般名フィルグラスチム)です。
グランの主成分であるフィルグラスチムは、遺伝子組換えの技術を用いて作られたG-CSFと呼ばれるタンパク質です。
G-CSF製剤には、骨髄中で好中球のもとになる細胞(前駆細胞)の増殖をさかんにするとともに、好中球の働きを強める作用があります。
このため、好中球が少なくなった患者さんがこの薬の投与を受けると、好中球が増え、感染に対する抵抗力が強くなることが期待されます。
グランが承認を受けた適応症はいくつかありますが、臨床の場で最も多く使われているのが、がん化学療法に伴う副作用の1つである「好中球減少症」の改善です。
「がん化学療法による好中球減少症」を適応症とした薬の使い方は、がんの種類によって(1)急性白血病(2)悪性リンパ腫、小細胞肺がん、胚細胞腫瘍(精巣腫瘍、卵巣腫瘍など)、神経芽細胞腫、小児がん(3)その他のがん―の大きく3つに分けられます。
(1)と(2)は、抗がん剤の治療で治癒する可能性が高いので、強い化学療法が行われます。そのため、好中球減少症が高い頻度で起こることがわかっています。そこで、抗がん剤治療後、好中球が減少する前に、予防的にグランを使い始めます。
(3)のその他のがんの化学療法では、好中球減少症が必ず起きるとは限りません。そこで、抗がん剤の治療を行い、好中球数が血液1マイクロリットルあたり1000個未満になって38度以上の発熱がある場合、あるいは好中球数が同様に500個未満になった場合に、グランが使われます。
この薬は、がん化学療法による好中球減少症以外に、白血病で造血幹細胞移植が行われるときにも使われています。移植後、好中球が徐々に増えていくときに、助ける働きをしてくれるのです。また、エイズや骨髄異形成症候群や再生不良性貧血による好中球減少症、先天性・特発性好中球減少症の治療にも使われています。
計画通りに化学療法を行うことが最も大事
「がん化学療法による好中球減少症」に対するグランの有効性については、次に示す効果などが臨床試験の結果により、得られています。
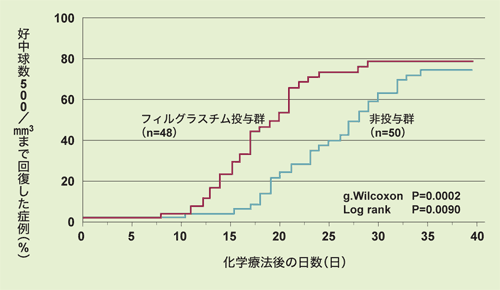
急性白血病における効果では、好中球数の回復に要する期間を短縮しました。これは、急性白血病の寛解導入療法後に、グラン投与群と非投与群とを比較した臨床試験で得られたものです。
こうした臨床試験の結果からもわかるように、抗がん剤治療時にグランを使うことで、抗がん剤による好中球の減少を防ぐことができ、好中球数の回復の期間を短縮することが可能になります。
しかし、グランを使うことの最大の目的は、好中球の減少を防ぐことや、好中球数を回復させることそのものではなく、これらを通じて抗がん剤の投与量を減らしたり、投与間隔を延ばすなどといった治療スケジュールの変更をしたりせずに、化学療法を計画通りに行うことです。
なぜなら、がんの化学療法は、臨床試験でその効果が確認されていますが、化学療法の効果を得るためには、決められた量を計画通りの日程で投与する必要があります。投与量や投与日程が変われば、臨床試験と同様の効果を得られる保証はありません。グランは、計画通りに化学療法を遂行し、エビデンス(科学的根拠)に基づいた効果を得るための薬なのです。
また、あらかじめ充填されたプレフィルドシリンジ(薬剤充填済み注射器)製剤は患者さんにとってより安全である点からも抗がん剤治療を受けるがん患者さんをサポートしています。
グランはもともとヒトが持っているG-CSFを遺伝子組換え技術を用いて製剤化したものですが、副作用もあります。主な副作用は、骨の痛み(とくに胸、腰、骨盤の骨)と発熱です。どちらも薬の主作用に伴って生じるもので、効いているからこそ起こる症状だといえます。これらは鎮痛剤、もしくは薬(グラン)の投与をやめれば改善します。
効果が長時間持続する第2世代の注射薬を開発中
グランは日本で1991年に承認されて以来(欧米でも承認済)、がんの化学療法を受ける患者さんに、広く使われてきました。
化学療法はかつて入院治療が普通でしたが、最近は通院で治療を受ける患者さんが増えています。しかし、好中球減少症が起きた場合、グランは注射薬なので、投与のために連続して通院する必要が生じます。グランを投与するための通院は患者さんにとっても負担ですし、交通機関内や病院などでの感染リスクが生じてしまいます。
そこで、1回の投与で、グランの効果が長時間持続する第2世代の注射薬の開発が日本で進められています。グランと同様の「がん化学療法による好中球減少症」の適応症で、欧米ではすでに「ニューラスタ(一般名ペグフィルグラスチム)」の商品名で発売中です。日本では現在、第2相臨床試験が行われている段階です。この新しいロングアクティブ注射薬が実用化されると、通院化学療法のメリットを最大限に生かすことができるようになります。
同じカテゴリーの最新記事
- 皮膚T細胞リンパ腫の新治療薬 タルグレチン(一般名ベキサロテン)
- EGFR遺伝子変異陽性非小細胞肺がんの治療薬 イレッサ(一般名ゲフィチニブ)/タルセバ(一般名エルロチニブ)/ジオトリフ(一般名アファチニブ)/タグリッソ(一般名オシメルチニブ)
- 前立腺がん骨転移の治療薬 ゾーフィゴ(一般名ラジウム-223)/ランマーク(一般名デノスマブ)/ゾメタ(一般名ゾレドロン酸)/メタストロン(一般名ストロンチウム-89)
- GIST(消化管間質腫瘍)の治療薬 グリベック(一般名イマチニブ)/スーテント(一般名スニチニブ)/スチバーガ(一般名レゴラフェニブ)
- 慢性リンパ性白血病の治療薬 FCR療法(フルダラ+エンドキサン+リツキサン)/アーゼラ(一般名オファツムマブ)/マブキャンパス(一般名アレムツズマブ)
- 悪性軟部腫瘍(軟部肉腫)の治療薬 アドリアシン(一般名ドキソルビシン)+イホマイド(一般名イホスファミド)/ヴォトリエント(一般名パゾパニブ)/ヨンデリス(一般名トラベクテジン)
- 悪性神経膠腫の治療薬 テモダール(一般名テモゾロミド)/アバスチン(一般名ベバシズマブ)/ギリアデル(一般名カルムスチン)
- 切除不能膵がんの治療薬 FOLFIRINOX療法/アブラキサン+ジェムザール併用療法
- 閉経前ホルモン受容体陽性乳がんの治療薬 抗エストロゲン薬(ノルバデックス)/LH-RHアゴニスト(リュープリン、ゾラデックス)
- B細胞性リンパ腫の治療薬 R-CHOP療法(リツキサン+エンドキサン+アドリアシン+オンコビン+プレドニン)/VR-CAP療法(ベルケイド+リツキサン+エンドキサン+アドリアシン+プレドニン)



