分子標的薬の使う順番の検討や併用が今後の課題 さらに進化している進行非小細胞肺がんの最新化学療法

がんの中でも予後が悪い肺がん。その中で驚くほど生存率を伸ばしてきたのが、手術不能または再発した、つまり進行した非小細胞肺がんの治療だ。
分子標的薬や免疫チェックポイント阻害薬などの新薬が相次いで登場し、遺伝子解析により〝効く人に効く〟薬剤を選択できる個別化医療が進化しつつある。さらに、治療薬の組み合わせによる臨床試験も世界規模で行われている。進行非小細胞肺がんにおける化学療法の最新情報を、日本医科大学付属病院がん診療センター長の久保田馨さんに伺った。
まずドライバー遺伝子を調べ、治療法確定へ
がん細胞のタンパク質の分子を標的とする分子標的薬。今日、がん化学療法の大きな柱となっているこの治療が、肺がんで最初に承認されたのは2002年、イレッサ(一般名ゲフィチニブ)だった。
日本人の肺がんの80%以上を占める非小細胞肺がんでは、細胞の表面に増殖に関係するEGFR(上皮成長因子受容体)というタンパク質が多く存在している。そして、EGFR遺伝子に変異が起こると、チロシンキナーゼ(TK)という酵素の働きが強化され、増殖のスイッチが入ったままになり、がん細胞がどんどん増えてしまう。そこで、この部位に結合する薬剤を送り込み、酵素の働きを抑えて増殖を防ぐ。
イレッサはこの遺伝子に変異がある(EGFR変異陽性)手術不能または再発した非小細胞肺がんに承認されている。このイレッサと、2007年に承認されたタルセバ(同エルロチニブ)を、EGFR変異陽性手術不能または再発非小細胞肺がんを対象とした分子標的薬(EGFRチロシンキナーゼ阻害薬:TKI)の第1世代と呼ぶ。
同様の薬剤は現在第3世代まで開発されていて、第2世代は2014年に承認されたジオトリフ(同アファチニブ)と昨年(2019年)承認されたビジンプロ(同ダコミチニブ)、第3世代が2016年に承認され、2018年に進行非小細胞肺がんの初回治療にも使えるように適応拡大されたタグリッソ(同オシメルチニブ)だ(図1)。
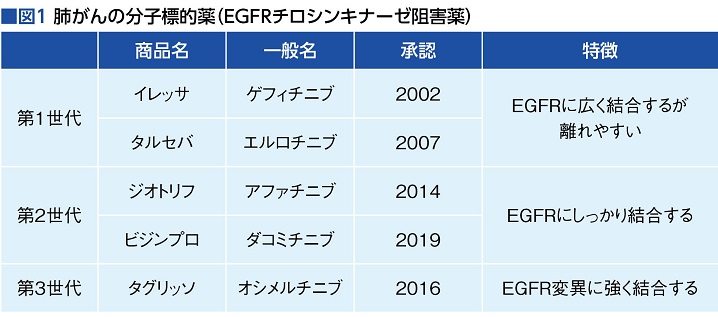
イレッサはまた、がん発生の直接原因となるような遺伝子の変異や転座(ドライバー遺伝子)を起こした細胞の阻害薬という点でも、分子標的薬の先駆となった。今日、がんの遺伝子のさまざまな変異/転座をターゲットとする分子標的薬の試験が世界で多数行われているが、これらの薬剤は標的分子があるかどうかを確認する遺伝子検査を同時に進化させた。
今日、非小細胞肺がんで重要視され、治療に当たって遺伝子検査を行うのは4項目。EGFR遺伝子変異、ALK融合遺伝子、ROS1融合遺伝子、BRAF遺伝子変異だ。これに加えて、2015年に保険適用になった免疫チェックポイント阻害薬である抗PD-1/PD-L1阻害薬がターゲットとするタンパク質PD-L1が、がん細胞のどのくらいにあるかを調べるPD-L1検査も併せて実施されることが多い。
従来の細胞障害性抗がん薬も効果あり、併用試験も多数
日本肺癌学会が作成した『肺癌診療ガイドライン2019年版』にも、「Ⅳ期非小細胞肺癌」の項目に「サブグループ別の治療方針」という図が記載されている。
①ドライバー遺伝子変異/転座陽性
②PD-L1陽性細胞50%以上
③ドライバー遺伝子変異/転座陰性、PD-L1陽性細胞50%未満もしくは不明
という3つのカテゴリーが示され、①は各キナーゼ阻害薬(分子標的薬)、②は免疫チェックポイント阻害薬のキイトルーダ(一般名ペムブロリズマブ)または細胞障害性抗がん薬(抗がん薬)+免疫チェクポイント阻害薬(PD-1/PD-L1阻害薬)を使い、①②の分子標的薬または免疫チェックポイント単剤で効果が得られなくなった場合に、抗がん薬を使う治療方針が示されている。また、③に対しては、抗がん薬+免疫チェックポイント阻害薬を使う治療方針となっている。
「今は、これくらいは調べないといけないでしょうね。ドライバー遺伝子に変異や転座があるかどうか、PD-L1がどのくらいあるかによって使う薬剤を選ぶのは標準です。合う薬剤があったらそれを使い、なかったら従来の抗がん薬+免疫チェクポイント阻害薬を使う。
新しい薬剤が次々出てくるので、副作用が強めの抗がん薬は使いたくないと思われるかもしれませんが、例えば、EGFR陽性の方は抗がん薬の効果も比較的高く、大事な選択肢の1つです。古い薬剤のジェムザール(同ゲムシタビン)が非常によく効き、2年以上効果が続いているという方もいます。さらに、現在は分子標的薬や免疫チェックポイント阻害薬単独だけでなく、抗がん薬との併用の効果を確認する臨床試験が広く行われています」と、日本医科大学付属病院がん診療センター長の久保田馨さん。
つまり、進行した非小細胞肺がんの治療薬はかなり出揃っていて、単独だけでなく様々な組み合わせた投与の可能性も模索されているということだ。その中心がⅣ期であり、Ⅲ期の治療にも単独あるいは併用の様々な試験が行われているという。また、個別化治療の隙間に落ち込みかねない患者救済のため、新たな臨床試験を患者自身が立ち上げるという新しい試みも始まっているという。
第3世代EGFRチロシンキナーゼ阻害薬の全生存期間中央値が3年以上に
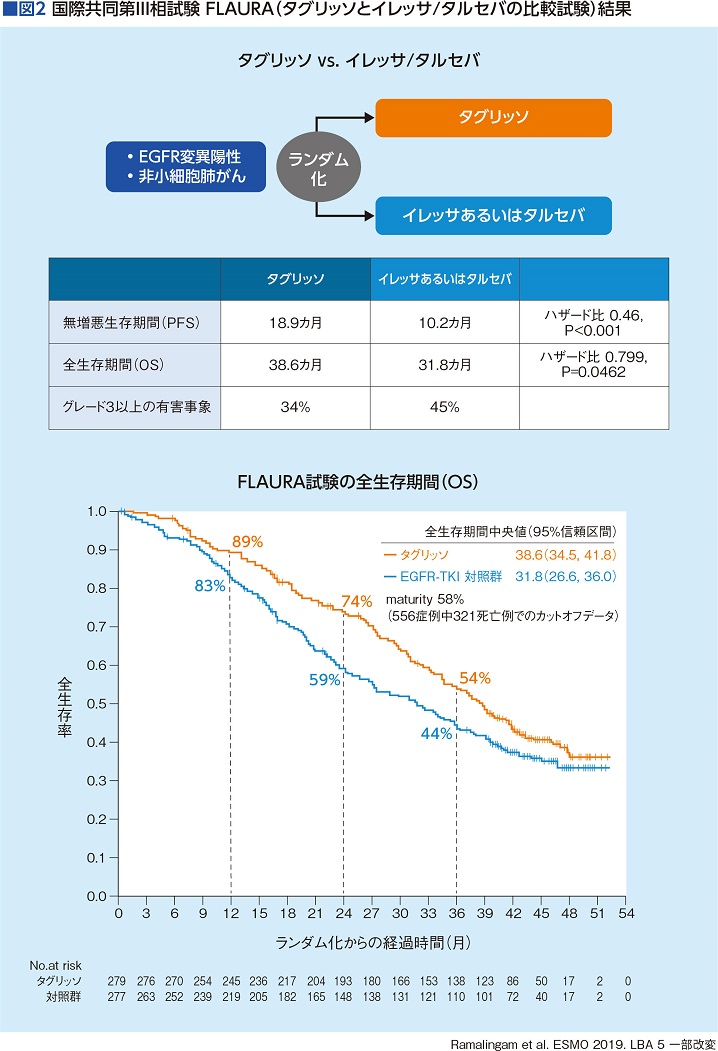
最新の進行非小細胞肺がん治療のニュースは、第3世代のEGFRチロシンキナーゼ阻害薬のタグリッソにまつわる話題だろう。未治療の局所進行または転移したEGFR遺伝子変異陽性非小細胞肺がん患者に対し、タグリッソを投与した群と、従来の標準治療である第1世代のイレッサまたはタルセバを投与した群を比較した、二重盲検国際共同第Ⅲ相試験(FLAURA試験)の最終結果が、昨年11月、欧州臨床腫瘍学会(ESMO2019)で発表された。
FLAURA試験の初回解析は2017年6月までのデータで行われており、無増悪生存期間(PFS)がタグリッソ群で18.9カ月、対照群で10.2カ月と有意な延長が認められていた。全生存期間(OS)のデータは未達(生存中)だったが、延長傾向が認められていた。また、安全性については対象薬とほぼ同様で、重篤な有害事象はタグリッソ群のほうが低かった。
EGFRチロシンキナーゼ阻害薬は投与して1、2年程度経つと耐性ができて効かなくなることが知られているが、タグリッソはEGFRチロシンキナーゼを阻害するだけでなく、この耐性をもたらす原因の1つであるT790Mの変異も阻害することが知られている。そのため、日本では2016年に耐性のできた患者を対象に保険承認され、2017年の初回解析で有効性と安全性が確認されたことから、2018年8月、初回治療にも適応が拡大されている。
そして今回、FLAURA試験の最終結果が報告され、副次評価項目の全生存期間中央値がタグリッソ群で38.6カ月、対照群が31.8カ月。3年を経過した時点で、タグリッソ群で279例中79例(28%)、対照群で277例26例(9%)が治療を継続していた(図2)。
同じカテゴリーの最新記事
- 免疫チェックポイント阻害薬の2剤併用療法が登場 肝細胞がんの最新動向と薬物療法最前線
- 新薬や免疫チェックポイント阻害薬も1次治療から 胃がんと診断されたらまずMSI検査を!
- リムパーザとザイティガの併用療法が承認 BRCA遺伝子変異陽性の転移性去勢抵抗性前立腺がん
- 免疫チェックポイント阻害薬で治療中、命に関わることもある副作用の心筋炎に注意を!
- SONIA試験の結果でもCDK4/6阻害薬はやはり1次治療から ホルモン陽性HER2陰性の進行・再発乳がん
- dose-denseTC療法も再脚光を ICI併用療法やADC新薬に期待の卵巣がん
- 心不全などの心血管の副作用に気をつけよう! 乳がんによく使われる抗がん薬
- 新規薬剤の登場でこれまでのサブタイプ別治療が劇的変化! 乳がん薬物療法の最新基礎知識
- 世界最大規模の画期的研究の一部解析結果が発表 大腸がんの術後補助療法の必要性をctDNAで判断する
- 「過剰検査・過剰治療の抑制」と「薬物療法の進歩」 甲状腺がん治療で知っておきたい2つのこと



