体にメスを入れず、がんだけを取り除く治療法 早期大腸がんなら、内視鏡治療(ポリペクトミー/EMR/ESD)で根治できる時代になった!

大腸の内視鏡的粘膜下層剥離術(ESD)が保険適用されて6年、その技術は今も進化し続けている。高度な技術を要するESDだが、合併症の発生率も徐々に低下し、「早期大腸がんは、内視鏡治療で根治できる」と言えるまでになってきた今、ESD症例数日本随一を誇るNTT東日本関東病院の内視鏡チームに話を聞いた。
内視鏡治療と手術の分かれ目は?
大腸がんを根治(こんち)させるには、がん細胞を取り除かなければならない。その方法としてまず挙げられるのは外科手術だ。腹部にメスを入れ、がん細胞ごと腸管を切除し、転移の可能性があるリンパ節を郭清(かくせい)、その後、腸管と腸管を吻合(ふんごう)して便が通る道を作り直すのが外科手術で、方法は開腹手術と腹腔鏡下手術の2通りがある。
腹部を大きく開く開腹手術に比べ、腹部に開けた孔(穴)から手術器具を挿入して行う腹腔鏡下手術は、傷も小さく、回復も早いというメリットはあるが、お腹の中で行うことはどちらも同じ。大腸の外側からアプローチし、腸管そのものを切除することに変わりはない。
大腸がん切除には、手術以外に、実はもう1つ方法があることを御存知だろうか。
それが、大腸の内視鏡治療だ。肛門から大腸内に挿入した内視鏡で、がんを切り取る治療法。つまり、大腸の内側からアプローチして、がん細胞だけを切除するため、腸管を切除せず、傷つけもしない。だから、後遺症もほとんどない、といういいこと尽くめの治療法なのだ。患者にしてみれば、人間ドックなどで行う大腸内視鏡検査を受けるのとほぼ同じ心構えで臨めるのだから、誰もが、内視鏡治療で大腸がんを切除したいと望むだろう。
しかし、「内視鏡治療ができるのは、リンパ節転移も含めて、転移の認められない早期大腸がんに限られます」とNTT東日本関東病院消化器内科医師の村元喬さんは語る。
腸管の内部からアプローチするため、内視鏡治療ではリンパ節郭清ができない。つまり、リンパ節転移が起きた時点で、内視鏡治療は適応外となってしまう。逆に言うと、がん細胞が粘膜下層(ねんまくかそう)の浅い層までに留まっていて、リンパ節転移を起こしていない段階ならば、内視鏡治療で大腸がんを根治させることができるのだ。
腸壁は、上から、粘膜、粘膜下層、筋層、漿膜(しょうまく)と4層構造になっていて、がん細胞は1番上の粘膜に発生する。そこから徐々に大きくなる過程で、腸壁に深く食い込んでいく(図1)。
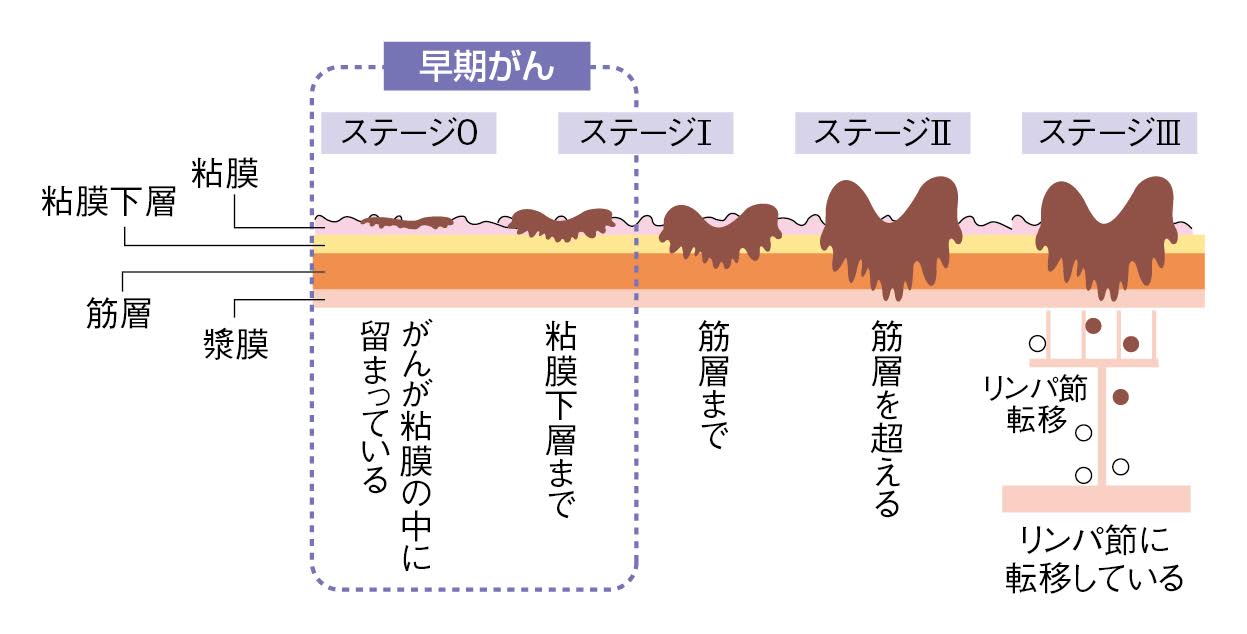
「内視鏡治療ができるかできないかの一番の分かれ目は、粘膜下層の浅い部分までに、がん細胞が留まっているかどうかです。粘膜下層の深いところまで浸潤(しんじゅん)していても技術的には内視鏡で切除できるのですが、たとえ切除できても、転移のリスクを残してしまう。それでは意味がありません」
つまり、重要なのは、がん細胞が腸壁のどこまで浸潤しているか。その「深さ」ということだ。ちなみに、内視鏡治療を行った際は、必ず切除した病変を病理検査に出して詳しく解析し、転移のリスクがないかを徹底的に調べる(病理診断)。リスクなしと出れば、その時点で根治となるが、リスクありと出たら、手術が必要となるそうだ。
ESDの登場と合併症
内視鏡治療の方法には、ポリペクトミー、EMR(内視鏡的粘膜切除術)、ESD(内視鏡的粘膜下層剥離術)の3種類がある。
最も早くから行われているのが、くびれ型や茎のある形の*ポリープに対して行われるポリペクトミー。スネアと呼ばれる金属製の輪を先端に取り付けた内視鏡を使って、ポリープを縛り、高周波電流を流して焼き切る方法(焼灼術)だ。がんだけでなく、良性ポリープや腺腫にも行われる。
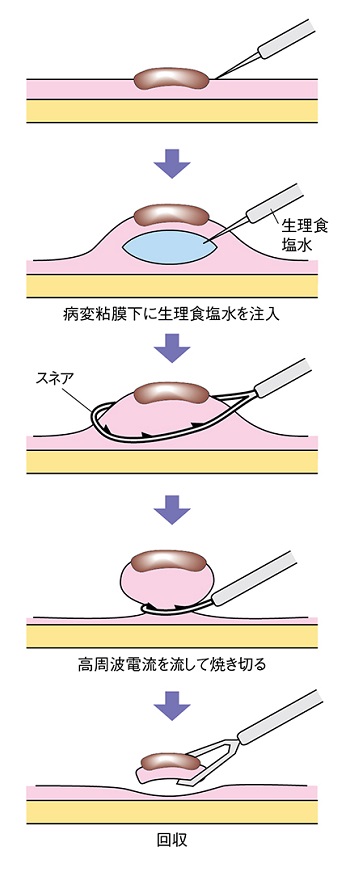
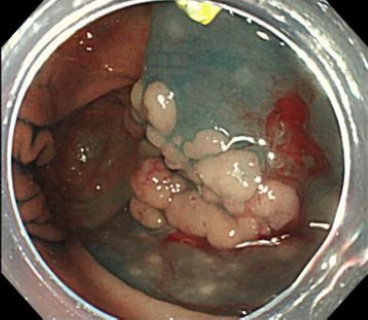
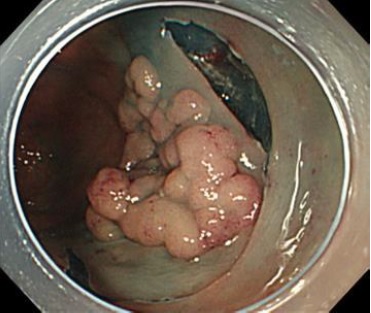
くびれや茎がなく、平坦、もしくは凹んでいる形の病変に対処できるよう考えられたのがEMR(図2)。
これは、スネアでポリープを縛れるようにするため、粘膜下層に生理食塩水を注入し、病変を浮き上がらせ、そこを、ポリペクトミーと同様、スネアで縛って焼き切る方法だ。
「ただし、スネアの輪の大きさを考えると、EMRで一括切除できるのは約2㎝まで。それを超えると昔は何回かに分けて切除するしかありませんでしたが、分割切除は取り残しを起こしやすく、再発リスクを高めます。その救世主となったのがESDでした」
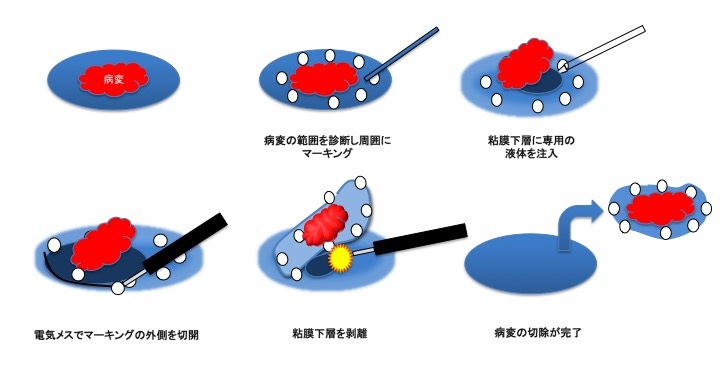
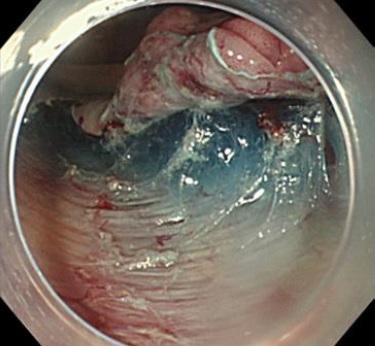
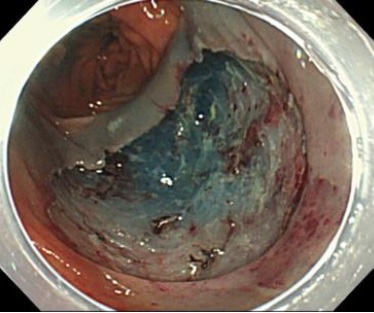
ESDは、〝一括切除2㎝〟の壁を破るべく、2000年に入ってから登場した内視鏡治療の最新治療法。病変の下の粘膜下層にヒアルロン酸を注入して病変を盛り上がらせるところまではEMRと同様だが、その後、スネアではなく、ボールペンのペン先ほどの極小の特殊な電気メスで、病変の周囲を切開し、粘膜下層から丁寧に剥がし取って一括切除する(図3)。
治療時間は、病変の大きさ、深さ、部位にもよるが、通常は30分から2時間ほど。入院期間は施設により多少異なるが、NTT東日本関東病院では、6日間で退院できるそうだ。
ちなみに、EMRでは生理食塩水を注入するのに、ESDではなぜヒアルロン酸なのかというと、ヒアルロン酸のほうが、粘膜の浮き上がりがよく、かつ、浮き上がっている時間が長く保てるから。EMRは2㎝以内の病変なので、生理食塩水で十分だが、電気メスを使い、治療時間が長くかかることが予想されるESDには、ヒアルロン酸のほうが適しているそうだ。
さて、2㎝を超える病変も一括切除できるようになったESDだが、EMRより大きく組織を切り取る分、粘膜下層の下の筋層に傷をつけたり(穿孔:せんこう)、術後の出血を引き起こすリスクが増える。つまり、医療的に高度な技量が問われる治療法であると言えるだろう。とくに、大腸は腸管の壁が3㎜程度と薄い上に、粘膜、粘膜下層、筋層、漿膜と4層に分かれており、粘膜下層だけでいうと、0.2~0.4㎜ほどの厚さなのだ。1㎜以内の中で病変の切除と剥ぎ取りを可能にするのは、かなりの技術を要することは想像に難くない。実際、ESDは2009年に先進医療指定を受け、2012年に保険収載されるまでの3年間は、先進医療扱いの治療だった。
ESDの合併症で主なものは、病変を切除したり、剥ぎ取っているときに起こる穿孔である。
「ミリ単位の狭いスペースでの剥ぎ取り作業は、病変の場所、大きさ、深さによっては、治療中にどうしても筋層まで傷が及んでしまうことがあります」と村元さんは言う。ただ、傷のつけ方、対処法が大事なのだそうだ。
胃酸の殺菌作用に守られている胃の内部と違い、大腸は下剤を使って便を輩出していても、どうしても腸管内に微量の便が残っている。ひどい穿孔を起こすと、大腸菌を含んだ便汁がお腹の中に漏れて、重症化すると腹膜炎を起こして緊急手術になることもあるそうだ。ちなみに、NTT東日本関東病院内視鏡チームでは、穿孔を起こす率は、現在1.9%。かつ、そのすべてが極小のもので、その場で医療用クリップで対処できるものだ、という。数年前まで3%だったが、ここ数年で1.9%にまで下げたそうだ。
その他の合併症としては、治療後の出血がある。血管は粘膜の至るところに走っているため、治療中の出血は必ず起こる。出血が起きたら、その都度、止血しながら治療を進めてゆき、病変剥離後、出血がない状態で治療終了となる。つまり、合併症としての出血とは、治療後、腸管内を食べ物が通ったり、便が通ったりして、腸が動くことで起きる出血だ。これも、同病院では現時点で1.0%。ほぼ、起こらないに等しい数値になっている。
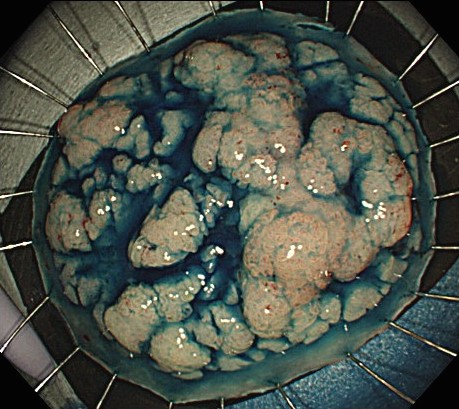
「大圃(NTT東日本関東病院内視鏡部部長)率いる内視鏡チームは現在10名。すべての患者さんのケースを10人でカンファレンスし、大圃の技術と考え方の元、意思統一しながら動いています。ですから、途中で治療法がぶれることは一切ないですし、技術も常に上を目指しています」と村元さん。ESDという治療が、いかに、医療者の力量に左右されるものかが窺える(写真4)。
同じカテゴリーの最新記事
- ヒト由来の人工皮膚使用で1次1期乳房再建が可能に! ダビンチSPで日本初の乳頭乳輪温存皮下乳腺全切除術
- 日本発〝触覚〟のある手術支援ロボットが登場 前立腺がんで初の手術、広がる可能性
- 薬物療法が奏効して根治切除できれば長期生存が望める ステージⅣ胃がんに対するコンバージョン手術
- 肛門温存の期待高まる最新手術 下部直腸がんTaTME(経肛門的直腸間膜切除術)とは
- 術後合併症を半減させたロボット支援下手術の実力 胃がん保険適用から3年 国産ロボット「hinotori」も登場
- 患者さんによりやさしいロボット手術も登場 新しくなった大腸がんの手術と薬物療法
- ガイドライン作成で内科的治療がようやく整理される コンセンサスがなかった食道胃接合部の食道腺がん
- 若手術者の養成が重要課題に 保険適用になった食道がんに対するダヴィンチ手術の現状
- 子宮体がんの最新治療と今後の可能性 免疫チェックポイント阻害薬を用いた治療が本格的にスタート!
- 増えているロボットによる腎がん部分切除 難しい腎がん部分切除を3DとVR技術を使ってより安全に



