- ホーム >
- 薬 >
- 免疫チェックポイント阻害薬
肺がん薬物療法最前線―― 分子標的薬と、オプジーボに代表される免疫チェックポイント阻害薬が、肺がん治療をここまで変えた!

EGFR遺伝子変異が、がん細胞の増殖に関わることが突き止められて10余年。いまや遺伝子変異検査によってがん細胞のタイプを見極め、自身のがん細胞の性格に合った薬物治療を受けられる時代になった。さらに、オプジーボに代表される免疫チェックポイント阻害薬の登場が、肺がん治療に新たな景色を見せ始めている――。
「がんと共に生きる」が現実になった
この15年、肺がん治療は目覚ましい進化を遂げた。始まりは、2002年の分子標的薬*イレッサの登場。とはいえ、このときはイレッサで劇的に病状が改善するケースがある一方、全く効果がないことも多く、かつ副作用が問題視されたりと、手探り状態だった。
2年後の2004年、がん細胞のEGFR遺伝子に変異が認められる場合にのみ、イレッサの効果が期待できることが判明。その後、がん細胞の遺伝子解析は年々進み、EGFR遺伝子変異に続き、ALK融合遺伝子、ROS1融合遺伝子と、がん細胞増殖の引き金となる遺伝子変異が次々と突き止められた。そして、遺伝子変異のタイプごとに、それぞれに見合う分子標的薬が登場。治療法も着実に確立されてきた。
さらに2015年末には、自身の免疫細胞ががん細胞を攻撃するよう働きかける免疫チェックポイント阻害薬が加わり、肺がん治療は新たな時代を迎えることとなる。
「10数年前までは、進行性肺がんには化学療法しか方法がなく、たとえ化学療法が効いても、ほとんどの場合、副作用で苦しんで苦しんで、最終的には短期間で命を終えていました。ですから当時、『薬でコントロールしながら肺がんと共存しましょう』なんて言うと、どこか嘘っぽかったのです。それから10余年を経た今、肺がん治療は大きく進化し、患者さん1人ひとりのがん細胞の遺伝子情報を把握し、それぞれに合った治療(個別化治療)ができるようになりました。今は、『がんと共に生きる』が詭弁(きべん)ではなく、現実になったと言えるでしょう」
そう語るのは、がん研有明病院呼吸器内科部長の西尾誠人さん。文字通り、進行性肺がんと診断されても、薬でコントロールしつつ、長期間、自身の生活を送り続けることができるようになった、という。
では、現在、進行性の非小細胞肺がん(全体の85%)と診断されたら、実際にどのような治療過程を経るのだろうか。
「まず、がん細胞の遺伝子検査から始めます」と西尾さん。
遺伝子タイプを正確に把握して、的確な治療法を知るためだ。「遺伝子変異検査で陽性が出た時点で治療法が見える」とも言い換えられる。そのためには、がん細胞の組織をしっかり採取することが重要。治療ではなく、がん組織を採取するために手術を行うこともあるそうで、それほど最初の診断が大切だということだ。
EGFR遺伝子変異、ALK融合遺伝子、ROS1融合遺伝子を、それぞれ順を追って調べる。
「実は、もうすぐ新たにBRAF遺伝子変異検査も承認される予定です。承認後は、ROS1検査の後に、BRAF検査が加わります」と西尾さん。
遺伝子変異検査で陽性と出た時点で、それに対応する分子標的薬治療へ進むことになる。すべてが陰性の場合は、がん細胞のPD-L1発現を調べ、免疫チェックポイント阻害薬が使えるかを判断。PD-L1発現が50%以上ならば免疫チェックポイント阻害薬の*キイトルーダ、50%未満の場合は、まずは化学療法をしてから、2次治療で*オプジーボかキイトルーダへ進む、という流れになる(図1)。
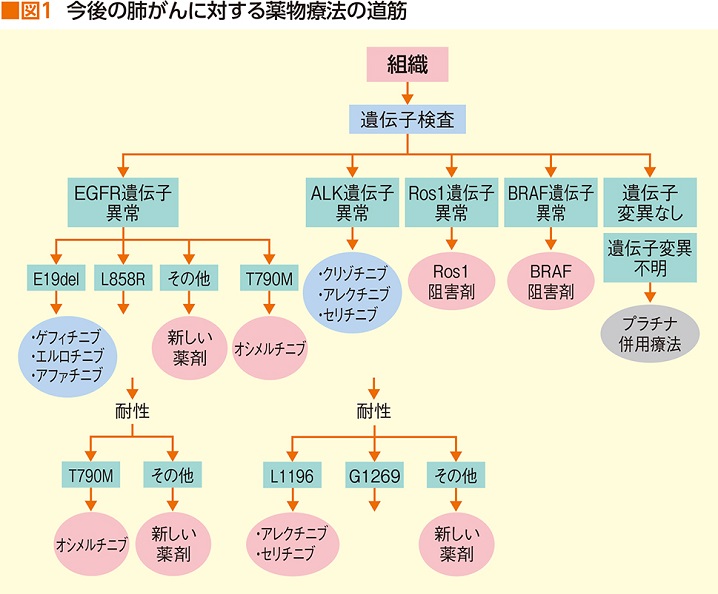
ちなみに現在、技術的には、すべての遺伝子変異検査を1回でできるようになったが、まだ保険適用外のため、一度ですべてを調べる検査は自費になる。EGFR遺伝子変異とALK融合遺伝子の同時検査は保険適用されたので、まずその2つを検査。陰性ならば、その先は、ROS1、PD-L1の順に、検査を進めていくが、場合により一度にこれらすべてを検査することもある。もちろん、最初に十分な量の組織を採取していれば、そこから少しずつ検査に出すので、何度も組織生検する必要はない。
遺伝子変異によるがん細胞増殖をストップ!
次に、分子標的薬、免疫チェックポイント阻害薬について、その仕組みと働きについて詳しく見ていこう。
肺がんにおいて、がん細胞増殖シグナルとして最初に発見されたのがEGFR遺伝子変異。がん細胞の細胞膜に突き刺さるように存在するEGFR遺伝子だが、このEGFR遺伝子に変異があると、細胞の外に位置する受容体に情報伝達物質が結合してがん細胞の増殖を促すシグナルを発信、がん細胞が加速度的に増えていくことがわかった。
非小細胞肺がんの約30%(腺がんの50%)にこのEGFR遺伝子異常が見られるため、最も高い確率で現われる変異と言っていいだろう。EGFR遺伝子変異のあるがん細胞に働きかけて、増殖指令の情報伝達物質が結合しないよう遮断するのがEGFR阻害薬 (EGFR-TKI)。イレッサ、*タルセバ(2007年承認)、*ジオトリフ(2012年承認)、そして*タグリッソ(2016年承認)がそれに当たる(図2)。
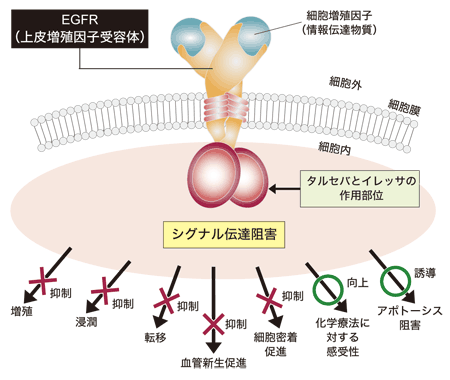
Pollack VA, et al. J Pharmacol Exp Ther 291: 739-48, 1999
ALK遺伝子とEML-4遺伝子が途中でちぎれてくっついて(=転座)できたALK融合遺伝子も、がん細胞を際限なく増殖させてしまう。そのスピードは通常の数百倍とも言われるほどで、非小細胞肺がんの約5%に発現する。ALK融合遺伝子が作り出す異常タンパクに働きかけて、がん細胞の増殖を抑えるのがALK阻害薬(ALK-TKI)だ。*ザーコリ(2012年承認)、*アレセンサ(2014年承認)、*ジカディア(2016年承認)がある。
ROS1融合遺伝子もALK融合遺伝子と同様に、ROS1遺伝子と他の遺伝子が転座してできる特殊な遺伝子。非小細胞肺がんの1~2%に発現する。ROS1融合遺伝子が作るROS1融合タンパクが、がん細胞の増殖を拡大するため、ROS1阻害薬(ROS1-TKI)でその作用を抑えるという仕組み。現在承認されているのはザーコリのみだ。
「ただし、どのタイプにせよ、薬が効かなくなる(耐性)時期がやってきます」と西尾さん。
その理由は様々だが、EGFR遺伝子を例にとると、大きく分けて2つの理由が考えられるという。
1つ目は、EGFR遺伝子の特定の場所に新たな遺伝子変異が起こり、イレッサやタルセバが結合しなくなることで起こる耐性。その新たな変異をT790M遺伝子変異と呼び、すでにT790Mにぴったり結合する新たな分子標的薬が2016年に登場した。それがタグリッソだ。つまり、T790M変異による耐性はタグリッソが解決してくれたわけだが、タグリッソもいずれは耐性ができることは避けられない。
2つ目は、イレッサやタルセバがEGFR遺伝子に結合してがん増殖シグナルを止めるものの、別ルートから、増殖シグナルが伝えられてきてしまうことによる耐性だ。バイパスシグナルの活性化と言い、これに対する方策は、血管新生阻害薬の*アバスチン(2009年承認)や、免疫チェックポイント阻害薬のオプジーボ、そして新たなバイパスシグナルを阻害する薬剤などとの併用が、今後期待されている。
【分子標的薬/EGFR阻害薬】 *イレッサ=一般名ゲフィチニブ *タルセバ=一般名エルロチニブ *ジオトリフ=一般名アファチニブ *タグリッソ=一般名オシメルチニブ
【分子標的薬/ALK阻害薬】 *ザーコリ=一般名クリゾチニブ *アレセンサ=一般名アレクチニブ *ジカディア=一般名セリチニブ
【免疫チェックポイント阻害薬】 *オプジーボ=一般名ニボルマブ *キイトルーダ=一般名ペムブロリズマブ
【抗がん薬と血管新生阻害薬】 *プラチナ系製剤=シスプラチン(商品名ブリプラチン/ランダ)やパラプラチン(一般名カルボプラチンなど) *アリムタ=一般名ペメトレキセド *アバスチン=一般名ベバシズマブ
同じカテゴリーの最新記事
- 免疫チェックポイント阻害薬との併用療法で大きく前進 新たな進行期分類が登場した子宮体がんの現在
- 免疫チェックポイント阻害薬で治療中、命に関わることもある副作用の心筋炎に注意を!
- キイトルーダ登場前の時代との比較データから確認 進行性尿路上皮がんの予後が大幅に延長!
- 肺がんに対する免疫チェックポイント阻害薬の治療効果は腸内細菌が関係!
- 複合がん免疫療法が、がん薬物療法の主力に! 免疫療法の個別化医療を目指す
- 胃がん新ガイドライン「条件付き承認」で増える治療選択 1次治療でオプジーボ承認
- 乳がん治療にも免疫チェックポイント阻害薬が登場! トリプルネガティブ乳がんで承認、さらに――
- 初期治療から免疫チェックポイント阻害薬選択の時代へ 腎細胞がん治療はここまで来た!
- 患者にもわかりやすく明確化された推奨する治療・しない治療 全面改訂された「大腸癌治療ガイドライン」2019年版
- 肺がんⅢ期の化学放射線療法後にイミフィンジが効果 放射線副作用の肺臓炎をいかに抑えるかが重要



